
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转换关系(为配平):
①G→Q+NaCl
②Q+H2O →X+H2
③ Y+NaOH →G+Q+H2O
④Z+NaOH→Q+X+H2O
这五种化合物中 氯的化合价由低到高的顺序为
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
科目:高中化学 来源:2016-2017学年海南省高二上期中文化学卷(解析版) 题型:选择题
变质的油脂有难闻的哈喇味,这是因为发生了
A.氧化反应 B.加成反应 C.还原反应 D.水解反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考文化学卷(解析版) 题型:选择题
通入水中所得溶液呈碱性的气体是
A.NH3 B.NO2 C.SO2 D.HCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:选择题
在密闭容器中发生反应mA(g)+nB(g)==pC(g),达到平衡后保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是( )[来源
A.m+n>p B.平衡向逆反应方向移动
C.A的转化率提高 D.C的体积分数增加
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:选择题
甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为2CH3OH+3O2+4OH-===2CO32-+6H2O。则下列说法正确的是 ( )
A.电池放电时通入空气的电极为负极
B.电池放电时负极的电极反应式为CH3OH-6e-+H2O===CO2↑+6H+
C.由于CO32-水解显碱性,电池放电时,电解质溶液的pH逐渐增大
D.电池放电时每消耗1 mol CH3OH转移6 mol电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上期中化学卷(解析版) 题型:选择题
下列离了方程式,正确的是
A.氢氧化铁与盐酸反应:H++OH-=H2O
B.少量CO2通入澄清石灰水使其变浑浊:CO2+Ca2++2OH-=CaCO3↓+H2O
C.铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑
D.CaCO3溶于稀盐酸中:CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A.分了数不同的CO与N2的体积一定不等
B.体枳相同的CO与N:的质量相等
C.质量相同、密度不同的CO与凡N2所含的原了数目—定相等
D.质量不同、密度相同的CO与N2所含分了数可能相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省、醴陵四中高二上期中化学卷(解析版) 题型:选择题
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A .使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.水电离的c(H+)=1×10﹣13 mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
C.Kw/c(H+)=1×10﹣13mol•L﹣1的溶液中:NH4+、Ba2+、Cl﹣、NO3﹣
D.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源:2017届陕西西安市高三上模拟三化学试卷(解析版) 题型:实验题
乳酸亚铁([CH3CH(OH)COO]2Fe.3H2O,Mr=288)是一种常用的补铁剂,可通过是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O+CO2↑。
已知FeCO3易被氧化:4FeCO3+6H2O+O2=4Fe(OH)3+4CO2。
某兴趣小组用FeCl2(用铁粉和稀盐酸制得)和NH4HCO3制备FeCO3的装置示意图如下:
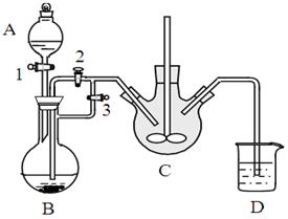
回答下列问题:
(1)NH4HCO3盛放在装置 中(填字母),该装置中涉及的主要反应的离子方程式____________。
(2)将生成的FeCl2溶液和NH4HCO3溶液混合时的操作是_________________。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。铁粉的作用是________,
反应结束后,无需过滤,除去过量铁粉的方法是 。
(4)该兴趣小组用KMnO4法测定样品中亚铁含量进而计算产品中乳酸亚铁的质量分数,高锰酸钾标准液用_________滴定管盛装(填“酸式”或“碱式”)。下列操作会引起测定结果偏高的是_________。
A.滴定管在盛装高锰酸钾前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.滴定前读数正确,滴定终点时仰视读数
(5)经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)2 19.70mL。滴定反应如下:Ce4++Fe2+=Ce3++Fe3+,则产品中乳酸亚铁的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com