
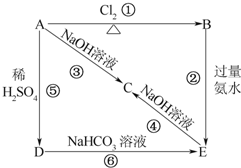
 图示中,E是不溶于水的白色胶状物质.
图示中,E是不溶于水的白色胶状物质.分析 A能与硫酸、氢氧化钠反应,则A为两性物质,且A能与氯气反应,故A为Al,可知B为AlCl3,氯化铝与氨水反应生成生成氢氧化铝与氯化铵,且E是不溶于水的白色胶状物质,则E为Al(OH)3,氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,则C为NaAlO2,Al与硫酸反应生成硫酸铝与氢气,而D能与碳酸氢钠反应生成E(氢氧化铝),故D为Al2(SO4)3,据此解答.
解答 解:(1)A能与硫酸、氢氧化钠反应,则A为两性物质,且A能与氯气反应,故A为Al,可知B为AlCl3,氯化铝与氨水反应生成生成氢氧化铝与氯化铵,且E是不溶于水的白色胶状物质,则E为Al(OH)3,氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,则C为NaAlO2,Al与硫酸反应生成硫酸铝与氢气,而D能与碳酸氢钠反应生成E(氢氧化铝),故D为Al2(SO4)3,
故答案为:Al;AlCl3;NaAlO2;
(2)反应①是Al与氯气反应生成氯化铝,反应化学方程式为:2Al+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2AlCl3,
反应②是氯化铝与氨水反应生成氢氧化铝沉淀与氯化铵,属于离子反应,反应离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
反应③是Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,属于离子反应,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
反应④是氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,属于离子反应,反应离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
反应⑤是Al与硫酸反应生产了硫酸铝与氢气,属于离子反应,反应离子方程式为:2Al+6H+=2Al3++3H2↑,
反应⑥是硫酸铝溶液与碳酸氢钠溶液发生双水解反应生成氢氧化铝沉淀、硫酸钠、二氧化碳,属于离子反应,反应离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,
故答案为:2Al+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2AlCl3;Al3++3NH3•H2O=Al(OH)3↓+3NH4+;2Al+2OH-+2H2O=2AlO2-+3H2↑;Al(OH)3+OH-=AlO2-+2H2O;2Al+6H+=2Al3++3H2↑;Al3++3HCO3-=Al(OH)3↓+3CO2↑.
点评 本题考查无机物推断,涉及Al元素单质化合物性质与转化,A发生的反应S推断突破口,再结合转化关系推断,侧重对化学方程式的考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | C2H6与C3H8没有同分异构体,CH2O2与C2H4O2属于同系物 | |
| B. | 一定条件下,乙酸乙酯、淀粉、蛋白质、乙烯都能与水发生水解反应 | |
| C. | 一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,则生成水的质量为18(1-a)g | |
| D. | 全降解塑料( 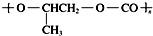 )可由单体环氧丙烷( )可由单体环氧丙烷(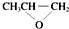 )和CO2缩聚制得 )和CO2缩聚制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含质子数=Z-n | B. | 所含中子数=A-Z+n | ||
| C. | 质量数=A+n | D. | 所含电子数=Z+n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙酸都能与金属钠反应 | |
| B. | 用氢氧化钠除去乙酸乙酯中的少量乙酸 | |
| C. | 植物油和动物脂肪都不能使溴水褪色 | |
| D. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在同温同压时,相同体积的任何气体单质所含的原子数目相同 | |
| B. | 2 g 氢气所含原子数目为 NA | |
| C. | 在常温常压下,11.2 L 氮气所含的原子数目为 NA | |
| D. | 17 g 氨气所含电子数目为 10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离出的c(H+) 减小 | B. | c(OH-) 与 c(H+) 的乘积增大 | ||
| C. | c(H+ ) 减小 | D. | c(OH-) 增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com