
元素周期表和元素周期律对化学学习具有指导意义,下列有关叙述正确的是( )
A.铅位于周期表中金属与非金属元素交界处,可做半导体材料
B.若存在简单阴离子R2-,则R一定属于第ⅥA族元素
C.S和Se属于第ⅥA族元素,H2S还原性比H2Se的强
D.元素原子最外层电子数较少的金属一定比最外层电子数较多的金属活动性强
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014年高考化学苏教版总复习 7-1 化学反应速率练习卷(解析版) 题型:选择题
已知汽车尾气无害化处理反应为2NO(g)+2CO(g) N2(g)+2CO2(g),下列说法不正确的是 ( )
N2(g)+2CO2(g),下列说法不正确的是 ( )
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高正反应速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 6-2 原电池、常见的化学电源练习卷(解析版) 题型:选择题
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是( )
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.氢氧燃料电池工作时氢气在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-2 元素周期律 元素周期表练习卷(解析版) 题型:填空题
现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素的性质或原子结构 |
X | 最外层电子数是次外层电子数的3倍 |
Y | 常温下单质是双原子分子,其氢化物的水溶液显碱性 |
Z | 第三周期元素的简单离子中半径最小 |
(1)元素X的一种单质在生活中常用作饮水机的消毒剂,该单质的化学式是 ,元素Z的离子结构示意图为 。
(2)元素Y与氢元素形成一种离子YH4+,请写出检验溶液中存在该离子的实验操作、现象和结论 。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式: 。
(4)元素X与元素Y相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.Y的氢化物可在纯X2中燃烧生成X的氢化物和Y2
b.X的单质比Y的单质更容易与H2化合
c.X与Y形成的化合物中Y元素呈正价态
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-2 元素周期律 元素周期表练习卷(解析版) 题型:选择题
短周期元素A、B、C、D在周期表中所处的位置如图所示。A、B、C、D四种元素的质子数之和为36。E元素原子的半径在同周期中最大,且E的离子与C的离子具有相同的电子层结构。则下列说法正确的是( )
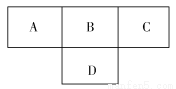
A.元素A形成的气态氢化物一定是正四面体形分子
B.五种元素形成的氢化物中,C的氢化物的沸点最高
C.A、C两种元素可形成A3C2型化合物,该化合物在空气中不能燃烧
D.B、C、D、E四种元素的离子半径由大到小的顺序为D>B>C>E
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-1 人类对原子结构的认识练习卷(解析版) 题型:填空题
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。
元素信息
B其单质在常温下为双原子分子,与A可形成分子X,X的水溶液呈碱性
D其简单阳离子与X具有相同电子数,且是同周期中简单阳离子中半径最小的
E元素原子最外层比次外层少2个电子
C、F两种元素的原子最外层共有13个电子
则(1)B的原子结构示意图为 。
(2)B、C、E分别与A形成的化合物中最稳定的是 (写化学式)。
(3)C与D形成的化合物的化学式是 ,它的性质决定了它在物质的分类中应属于 ;请写出该化合物对应水化物电离的方程式 。
(4)F的单质在反应中常作 剂,该单质的水溶液与E的低价氧化物反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-1 人类对原子结构的认识练习卷(解析版) 题型:选择题
A和B是短周期元素,A2-与B+的核外电子总数之差为8,则下列说法正确的是( )
A.A和B的原子序数之差为8
B.A和B原子的最外层电子数之和为8
C.A和B原子的最外层电子数之差为7
D.A和B原子的核外电子数总和可能为11
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 3-3 含硅矿物与信息材料练习卷(解析版) 题型:选择题
200°C时,11.6克CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体的质量增加了3. 6克。从以上信息中,我们得出的下列结论中不正确的是( )
A.可以计算出混合气体中CO2和水蒸气的质量
B.可以判断出混合气体的平均摩尔质量
C.可以计算出该反应中转移的电子数
D.可以总结出Na2O2任何反应中既作氧化剂也作还原剂
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 2-2 钠、镁及其化合物练习卷(解析版) 题型:实验题
有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的装置进行实验。通入SO2气体,将带火星的木条插入试管C中的溶液上方,木条复燃。

请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是 。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3: 。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
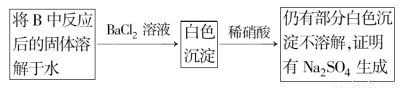
上述方案是否合理? 。请简要说明两点理由:① ;② 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com