
| A、普通玻璃的主要成分是纯碱、石灰石和二氧化硅 |
| B、标准状况下,1 mol Na2O2和22.4LSO2反应,转移电子数目为2NA |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
| D、C、S分别在空气中燃烧均可得到两种不同的氧化物 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、将铜粉和硫粉混合均匀并加热以制取CuS |
| B、将Cu片放入过量浓硫酸中,一段时间后加水以观察CuSO4溶液的颜色 |
| C、向CuSO4溶液中加入NaOH溶液,过滤洗涤并收集沉淀,加热以制取CuO |
| D、设计Cu-Al-浓硝酸原电池,以证明金属活动性:Cu<Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 |
| 氨水 | KOH | K2CO3 |
| A、甲>乙>丙 |
| B、乙>甲>丙 |
| C、丙>乙>甲 |
| D、丙>甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
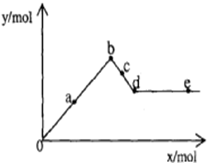 已知Ba(AlO2)2可溶于水.如图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述错误的是( )
已知Ba(AlO2)2可溶于水.如图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述错误的是( )| A、d-e 时溶液中离子的物质的量:Ba2+可能等于AlO2- |
| B、b-c 时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C、a-d 时沉淀的物质的量:Al(OH)3一定小于BaSO4 |
| D、a-b 时沉淀的物质的量:Al(OH)3比BaSO4多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③⑤ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原剂 |
| B、氧化剂 |
| C、既是还原剂又是氧化剂 |
| D、既不是氧化剂又不是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com