
ĻĀĮŠŅĄ¾ŻČČ»Æѧ·½³ĢŹ½µĆ³öµÄ½įĀŪÕżČ·µÄŹĒ£Ø£©
A£® ŅŃÖŖ2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=﹣483.6 kJ•mol﹣1£¬ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ•mol﹣1
B£® ŅŃÖŖNaOH£Øaq£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H=﹣57.3 kJ•mol﹣1£¬Ōņŗ¬40.0g NaOHµÄĻ”ČÜŅŗÓėĻ”“×ĖįĶźČ«ÖŠŗĶ£¬·Å³öŠ”ÓŚ57.3kJµÄČČĮæ
C£® ¼ŗÖŖ2C£Øs£©+2O2£Øg£©=2CO2£Øg £©”÷H=a£»2C£Øs£©+O2£Øg£©=2CO£Øg£©£»”÷H=b£¬Ōņa£¾b
£©”÷H=a£»2C£Øs£©+O2£Øg£©=2CO£Øg£©£»”÷H=b£¬Ōņa£¾b
D£® ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0£¬ŌņŹÆÄ«±Č½šøÕŹÆĪȶØ
æ¼µć£ŗ ČČ»Æѧ·½³ĢŹ½£®
×ØĢā£ŗ »Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ£®
·ÖĪö£ŗ A”¢ŅĄ¾ŻČ¼ÉÕČČøÅÄī·ÖĪö£¬1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮæ·ÖĪö£»
B”¢“×ĖįŹĒČõĖįµēĄė¹ż³ĢŹĒĪüČČ¹ż³Ģ£»
C”¢Ņ»Ńõ»ÆĢ¼Éś³É¶žŃõ»ÆĢ¼¹ż³ĢŠčŅŖ·ÅČČ£¬ģŹ±äĪŖøŗÖµ£»
D”¢ĪļÖŹÄÜĮæŌ½øßŌ½»īĘĆ£®
½ā“š£ŗ ½ā£ŗA”¢ŅŃÖŖ2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=﹣483.6 kJ•mol﹣1£¬·½³ĢŹ½ÖŠĖ®ŹĒĘųĢ壬ŅĄ¾ŻČ¼ÉÕČČøÅÄīæÉÖŖ£¬ĒāĘųµÄČ¼ÉÕČČ“óÓŚ241.8 kJ•mol﹣1 £¬¹ŹA“ķĪó£»
B”¢“×ĖįŹĒČõĖįµēĄė¹ż³ĢŹĒĪüČČ¹ż³Ģ£¬Ōņŗ¬40.0g NaOHµÄĻ”ČÜŅŗĪļÖŹµÄĮæĪŖ1mol£¬ÓėĻ”“×ĖįĶźČ«ÖŠŗĶ£¬·Å³öŠ”ÓŚ57.3kJµÄČČĮ棬¹ŹBÕżČ·£»
C”¢¼ŗÖŖ2C£Øs£©+2O2£Øg£©=2CO2£Øg£©”÷H=a£»2C£Øs£©+O2£Øg£©=2CO£Øg£©£»”÷H=b£¬Ņ»Ńõ»ÆĢ¼Éś³É¶žŃõ»ÆĢ¼¹ż³ĢŠčŅŖ·ÅČČ£¬ģŹ±äĪŖøŗÖµ£¬Ōņa£¼b£¬¹ŹC“ķĪó£»
D”¢ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0£¬½šøÕŹÆÄÜĮæøߣ¬ŌņŹÆÄ«±Č½šøÕŹÆĪČ¶Ø£¬¹ŹDÕżČ·£»
¹ŹŃ”BD£®
µćĘĄ£ŗ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½µÄŹéŠ“·½·ØŗĶøÅÄīĄķ½āÓ¦ÓĆ£¬Ö÷ŅŖŹĒČ¼ÉÕČČ£¬ÖŠŗĶČČøÅÄī·ÖĪöÓ¦ÓĆ£¬ĪļÖŹÄÜĮæøßµĶÓėĪļÖŹĪČ¶ØŠŌµÄ¹ŲĻµÅŠ¶Ļ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆ98%µÄÅØH2SO4£Ø¦Ń=1.84g£®cm﹣3£©ÅäÖĘ1mol/LµÄĻ”ĮņĖį100mL£¬°“ÅäÖĘČÜŅŗŹ±ŅĒĘ÷µÄŃ”ÓĆĖ³Šņ ÅÅĮŠ£¬Ń”ŌńÕżČ·µÄŹĒ£Ø£©
ÅÅĮŠ£¬Ń”ŌńÕżČ·µÄŹĒ£Ø£©
¢Ł²£Į§°ō ¢Ś½ŗĶ·µĪ¹Ü ¢Ū100mLČŻĮæĘæ ¢ÜĶŠÅĢĢģĘ½ ¢Ż50mLÉÕ± ¢Ž10mLĮæĶ² ¢ß100mLĮæĶ² ¢ąŅĘŅŗ¹Ü ¢įµĪ¶Ø¹Ü£®
A£® ¢Ž¢Ū¢ą¢Ż¢Ł¢Ś B£® ¢Ž¢Ż¢Ū¢Ł¢į¢Ś C£® ¢Ü¢Ż¢Ū¢Ś¢Ł¢į D£® ¢Ž¢Ż¢Ł¢Ū¢Ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅųÖĘĘ÷ĆóČÕ¾Ć±ķĆę»įÖš½„±äŗŚ£¬ÕāŹĒÉś³ÉĮĖAg2SµÄŌµ¹Ź£®øł¾Żµē»ÆѧŌĄķæɽųŠŠČēĻĀ“¦Ąķ£ŗŌŚĀĮÖŹČŻĘ÷ÖŠ¼ÓČėŹ³ŃĪČÜŅŗ£¬ŌŁ½«±äŗŚµÄŅųĘ÷½žČėøĆČÜŅŗÖŠ£¬Ņ»¶ĪŹ±¼äŗó·¢ĻÖŗŚÉ«»įĶŹČ„£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® “¦Ąķ¹ż³ĢÖŠŅųĘ÷Ņ»Ö±±£³ÖŗćÖŲ
B£® ŅųĘ÷ĪŖÕż¼«£¬Ag2S±»»¹ŌÉś³Éµ„ÖŹŅų
C£® øĆ¹ż³ĢÖŠ×Ü·“Ó¦ĪŖ2Al+3Ag2S═6Ag+Al2S3
D£® ŗŚÉ«ĶŹČ„µÄŌŅņŹĒŗŚÉ«Ag2S×Ŗ»ÆĪŖ°×É«AgCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
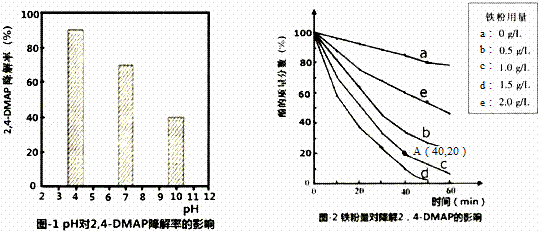
ĄūÓĆNa2S2O8²śÉśµÄĒæŃõ»ÆŠŌSO4﹣•£Ø×ŌÓÉ»ł£©½µ½āÓŠ»śĪŪČ¾ĪļŹĒÄæĒ°×ī¾ßĒ±Į¦µÄøß¼¶Ńõ»Æ¼¼Źõ£®ĪÄĻױصĄÄ³æĪĢā×éĢ½¾æpH£¬µ„ÖŹĢśŗĶNa2S2O8µÄÅØ¶Č¶Ō½µ½ā2£¬4﹣DMAP£Ø2£¬4﹣﹣¼×»ł±½·Ó£©Š§ĀŹµÄÓ°Ļģ£®
£Ø1£©Ģ½¾æČÜŅŗĖį¼īŠŌµÄÓ°Ļģ£ŗ½«µČĮæµÄ2£¬4﹣DMAP¼ÓČėµ½²»Ķ¬pHµÄNa2S2O8ČÜŅŗÖŠ£¬½į¹ūČēĶ¼1ĖłŹ¾£®ÓÉ“ĖæÉÖŖ£ŗČÜŅŗĖįŠŌŌöĒ棬 £ØĢī”°ÓŠĄūÓŚ”±»ņ”°²»ĄūÓŚ”±£©Na2S2O8²śÉśSO4﹣•£®
£Ø2£©Ģ½¾æĢś·ŪÓĆĮæµÄÓ°Ļģ£ŗ
¢ŁŹµŃéĒ°£¬ĻČÓĆ0.1mol•L﹣1 H2SO4Ļ“µÓFe·Ū£¬ĘäÄæµÄŹĒ £¬ŗóÓĆÕōĮóĖ®Ļ“µÓÖĮÖŠŠŌ£»
¢ŚĻąĶ¬Ģõ¼žĻĀ£¬Č”²»Ķ¬Į擦ĄķŗóµÄĢś·Ū·Ö±š¼ÓČėc£Ø2£¬4﹣DMAP£©=1.0”Į10 ﹣3mol•L﹣1”¢c£ØNa2S2O8£©=4.2”Į10﹣3mol•L﹣1µÄ»ģŗĻČÜŅŗÖŠ£¬ŹµŃé½į¹ūČēĶ¼2ĖłŹ¾£®ĘäÖŠ½µ½āŠ§ĀŹ×īŗƵÄĢś·ŪÓĆĮæŹĒ1.5g/L£»¼ĘĖć“Ó·“Ó¦æŖŹ¼µ½AµćŹ±£¬2£¬4﹣DMAP½µ½āµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £ØŗöĀŌ·“Ó¦¹ż³ĢÖŠČÜŅŗ×ÜÖŹĮæ±ä»Æ£©£®
¢ŪŅŃÖŖ£ŗ2Fe+O2+2H2O=2Fe2++4OH﹣£¬S2O8﹣+Fe2+=SO4﹣+SO42﹣+Fe3+“ĖĶā»¹æÉÄÜ»į·¢Éś£ŗSO4﹣+Fe2+=SO42﹣+Fe3+£®µ±Ģś·Ū¼ÓČėĮæ¹ż“óŹ±£¬2£¬4﹣DMAPµÄ½µ½āĀŹ·“¶ųĻĀ½µ£¬ŌŅņæÉÄÜŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©£® £®
£Ø3£©Ģ½¾æNa2S2O8ÅØ¶ČµÄÓ°Ļģ£ŗĢīŠ“ĻĀ±ķÖŠæÕøń£¬Ķź³ÉŹµŃé·½°ø£®
ŠņŗÅ”¢ĪļĄķĮæ M£ØFe·Ū£©/g V/mL V/mL ŹÕ¼ÆŹż¾ŻŗĶµĆ³ö½įĀŪ
1 100 0.3 50 50
2 100V£ØĪŪĖ®£©/mL 0.3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
2HI£Øg£©⇌H2£Øg£©+I2£Øg£©·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ØĶ¼ÖŠE1±ķŹ¾Õż·“Ó¦µÄ»ī»ÆÄÜ£¬E2±ķŹ¾Äę·“Ó¦µÄ»ī»ÆÄÜ£©£®ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø£©
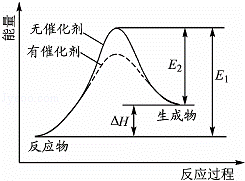
A£® ÉżøßĪĀ¶Č£¬·“Ó¦ĖŁĀŹŌö“󣬔÷H¼õŠ”
B£® ÉżøßĪĀ¶Č£¬²»Ó°Ļģ»ī»Æ·Ö×Ó°Ł·ÖŹż
C£® “߻ƼĮÄܽµµĶøĆ·“Ó¦µÄ»ī»ÆÄÜ
D£® Äę·“Ó¦µÄ»ī»ÆÄܵČÓŚÕż·“Ó¦µÄ»ī»ÆÄÜ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŹĀŹµÄÜĖµĆ÷Ó°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄ¾ö¶ØŠŌŅņĖŲŹĒ·“Ó¦Īļ±¾ÉķŠŌÖŹµÄŹĒ£Ø£©
A£® CuÄÜÓėÅØĻõĖį·“Ó¦£¬¶ų²»ÓėÅØŃĪĖį·“Ó¦
B£® CuÓėÅØĻõĖį·“Ó¦±ČÓėĻ”ĻõĖį·“Ó¦æģ
C£® N2ÓėO2ŌŚ³£ĪĀ”¢³£Ń¹ĻĀ²»·“Ó¦£¬·ÅµēŹ±æÉ·“Ó¦
D£® FeÓėÅØŃĪĖį·“Ó¦æģ£¬ÓėĻ”ŃĪĖį·“Ó¦Āż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ĢĢåNH4BrÖĆÓŚĆܱÕČŻĘ÷ÖŠ£¬Ä³ĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗNH4Br£Øs£©⇌NH3£Øg£©+HBr£Øg£©£¬2HBr£Øg£©⇌Br2£Øg£©+H2£Øg£©£¬2minŗó²āÖŖH2µÄÅضČĪŖ0.5mol•L﹣1£¬HBrµÄÅضČĪŖ4mol•L﹣1£¬ČōÉĻŹö·“Ó¦ĖŁĀŹÓĆv£ØNH3£©±ķŹ¾£¬ŌņĻĀĮŠĖŁĀŹÕżČ·µÄŹĒ£Ø£©
A£® 0.5mol•L﹣1•min﹣1 B£® 2.5mol•L﹣1•min﹣1
C£® 2mol•L﹣1•min﹣1 D£® 1.25mol•L﹣1•min﹣1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚČČ»Æѧ·“Ó¦µÄĆčŹöÖŠÕżČ·µÄŹĒ£Ø£©
A£® HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=﹣5 7.3 kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø﹣57.3£©kJ/mol
7.3 kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø﹣57.3£©kJ/mol
B£® Ģ¼Óė¶žŃõ»ÆĢ¼µÄ·“Ó¦¼ČŹĒĪüČČ·“Ó¦£¬ÓÖŹĒ»ÆŗĻ·“Ó¦
C£® ČČ»Æѧ·½³ĢŹ½ÖŠ»Æѧ¼ĘĮæŹżæɱķŹ¾·Ö×ÓøöŹż
D£® 1 mol¼×ĶéČ¼ÉÕÉś³ÉĘųĢ¬Ė®ŗĶ¶žŃõ»ÆĢ¼Ėł·Å³öµÄČČĮæŹĒ¼×ĶéµÄČ¼ÉÕČČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖA£Øg£©+B£Øg£©⇌C£Øg£©+D£Øg£©·“Ó¦µÄĘ½ŗā³£ŹżŗĶĪĀ¶ČµÄ¹ŲĻµČēĻĀ£ŗ
|ĪĀ¶Č/”ę 700 900 830 1000 1200
Ę½ŗā³£Źż 1.7 1.1 1.0 0.6 0.4
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦µÄ”÷H 0£ØĢī”°£¼”±”°£¾”±”°=”±£©£»
£Ø2£©830”ꏱ£¬ĻņŅ»øö5LµÄĆܱÕČŻĘ÷ÖŠ³äČė0.20molµÄAŗĶ0.80molµÄB£¬Čō·“Ó¦¾Ņ»¶ĪŹ±¼äŗ󣬓ļµ½Ę½ŗāŹ±AµÄ×Ŗ»ÆĀŹĪŖ80%£¬Čē¹ūÕāŹ±ĻņøĆĆܱÕČŻĘ÷ÖŠŌŁ³äČė1molė²Ęų£¬Ę½ŗāŹ±AµÄ×Ŗ»ÆĀŹ»į £ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©
£Ø3£©Čō±£³ÖČŻĘ÷µÄČŻ»ż²»±ä£¬ŌņøĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ £ØĢīŠņŗÅ£©£®
a£®µ„Ī»Ź±¼äĄļÉś³ÉBŗĶDµÄĪļÖŹµÄĮæĻąµČ
b£®ĘųĢåµÄĆÜ¶Č²»Ėꏱ¼äøıä
c£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
d£®»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ±£³Ö²»±ä
£Ø4£©1200”ꏱ·“Ó¦C£Øg£©+D£Øg£©⇌A£Øg£©+B£Øg£©µÄĘ½ŗā³£ŹżµÄ ÖµĪŖ £®
ÖµĪŖ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com