
 ČēĶ¼ĖłŹ¾ŹĒij»ÆѧŠĖȤŠ”×éĢ½¾æČÜŅŗÖŠĄė×ÓÅضČÓėČÜŅŗµ¼µēŠŌµÄ¹ŲĻµ£®
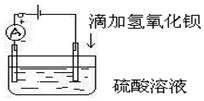
ČēĶ¼ĖłŹ¾ŹĒij»ÆѧŠĖȤŠ”×éĢ½¾æČÜŅŗÖŠĄė×ÓÅضČÓėČÜŅŗµ¼µēŠŌµÄ¹ŲĻµ£®·ÖĪö £Ø1£©ĻņH2SO4ČÜŅŗÖŠµĪ¼ÓBa£ØOH£©2ČÜŅŗ£¬·¢ÉśµÄ·“Ó¦ĪŖH2SO4+Ba£ØOH£©2=BaSO4”ż+2H2O£¬ČÜŅŗÓÉĮņĖįČÜŅŗ×Ŗ»ÆĪŖĖ®£¬ČÜŅŗĆÜ¶Č¼õŠ”£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č½µµĶ£¬ČÜŅŗµ¼µēÄÜĮ¦¼õŠ”£»
£Ø2£©ČÜŅŗµ¼µēŠŌ³żĮĖÓėĄė×ÓÅضČÓŠ¹Ų£¬»¹æÉÄÜÓėĄė×ÓĖł“ųµÄµēŗÉÓŠ¹Ų£®
½ā“š ½ā£ŗ£Ø1£©¢ŁĻņH2SO4ČÜŅŗÖŠµĪ¼ÓBa£ØOH£©2ČÜŅŗÖĮ·“Ó¦ĶźČ«£¬·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ2H++SO42-+Ba2++2OH-=BaSO4”ż+2H2O£¬
¹Ź“š°øĪŖ£ŗ2H++SO42-+Ba2++2OH-=BaSO4”ż+2H2O£»
¢ŚĖę×ÅĒāŃõ»Æ±µµÄµĪČė£¬ČÜŅŗÖŠĄė×ÓµÄÅضČÖš½„¼õŠ””¢ČÜÖŹÖš½„¼õÉŁ£¬µ¼µēÄÜĮ¦¼õČõ£¬µ±Į½ÖÖČÜŅŗĒ”ŗĆĶźČ«·“Ó¦Ź±£¬ČÜŅŗÖŠ¼øŗõƻӊ×ŌÓÉŅĘ¶ÆµÄĄė×Ó£¬ĖłŅŌµēĮ÷¼ĘĘ«×Ŗ³Ģ¶ČÖš½„¼õŠ”£¬×īŗóĪŖĮć£¬ŌŁ¼ÓČėĒāŃõ»Æ±µ£¬µĆµ½µÄŹĒĒāŃõ»Æ±µČÜŅŗ£¬µ¼µēÄÜĮ¦»įÖš½„ŌöĒ棬¹ŹŃ”A£»
£Ø2£©ČÜŅŗµ¼µēŠŌ³żĮĖÓėĄė×ÓÅضČÓŠ¹Ų£¬»¹æÉÄÜÓėĄė×ÓĖł“ųµÄµēŗÉÓŠ¹Ų£¬Ń”ĻīÖŠČÜŅŗÖŠµÄŃōĄė×ÓŹĒÄĘĄė×Ó”¢ĒāĄė×Ó”¢Ć¾Ąė×Ó£¬ŅõĄė×ÓŹĒ“×ĖįøłĄė×Ó”¢ĀČĄė×ÓŅŌ¼°ĮņĖįøłĄė×Ó£¬æÉŅŌŃ”Ōń“ųµēŗɲ»µČµÄĮņĖįĆ¾½ųŠŠŹŌŃ飬Ą“ŃéÖ¤Ąė×ÓĖł“ųµÄµēŗÉŗĶČÜŅŗµ¼µēÄÜĮ¦Ö®¼äµÄ¹ŲĻµ£¬¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲ»ÆŗĻĪļŠŌÖŹ¼°Ąė×Ó·“Ó¦”¢ČÜŅŗµ¼µēŠŌµČÖŖŹ¶µć£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·µ¼µēŠŌÓėĄė×ÓÅØ¶Č¹ŲĻµŹĒ½ā±¾Ģā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 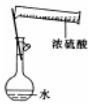 ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄĻ”ĮņĖį | B£® | 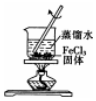 ÖĘȔɣĮæµÄFe£ØOH£©3½ŗĢå | ||
| C£® | 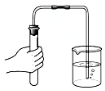 ¼ģ²éĘųĆÜŠŌ | D£® | 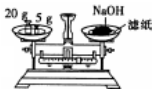 ³ĘĮæNaOH¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗ¶”£¾±ū£¾ŅŅ£¾¼× | |
| B£® | ŅŅŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖµŚČżÖÜĘŚµŚ¢ō×å | |
| C£® | 1molAÓė×ćĮæBĶźČ«·“Ó¦¹²×ŖŅĘ1molµē×Ó | |
| D£® | 1.0mol•L-1EČÜŅŗÖŠŅõĄė×Ó×ܵÄĪļÖŹµÄĮæŠ”ÓŚ0.1mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õō·¢ | B£® | Éż»Ŗ | C£® | ½į¾§ | D£® | ŻĶČ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬4g H2ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ 2NA | |
| B£® | 17g°±ĘųĖłŗ¬µē×ÓŹżÄæĪŖ8NA | |
| C£® | ½«1Ģå»żc1mol/LµÄĮņĖįČÜÓŚ4Ģå»żĖ®ÖŠ£¬Ļ”ČÜŅŗµÄÅضČĪŖ0.2c1mol/L | |
| D£® | ½«5.85gNaCl¾§ĢåČÜČė100mLĖ®ÖŠ£¬ÖʵĆ0.1mol/LµÄNaClČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com