
| A. | 二甲苯 | B. | 丁醇 | C. | 一氯丁烯 | D. | 二氯丙烷 |
分析 A、二甲苯的同分异构体中,可以是两个甲基连在苯环上,还可以是乙基连在苯环上;
B、丁基有四种,据此确定丁醇数目;
C、丁烯有3种同分异构体,分别是1-丁烯、2-丁烯、2-甲基-1-丙烯,然后依次分析三种烯烃满足题目要求结构的一氯丁烯;
D、二氯丙烷存在氯原子的位置异构.
解答 解:A、二甲苯的同分异构体中,可以是两个甲基连在苯环上,还可以是乙基连在苯环上,共4种;
B、丁基有四种,据此确定丁醇是四种;
C、丁烯有3种同分异构体,分别是1-丁烯、2-丁烯、2-甲基-1-丙烯,一氯丁烯存在官能团的位置异构,共8种;
D、二氯丙烷存在氯原子的位置异构,共四种.
化合物中同类别同分异构体数目最多的是C.故选C.
点评 本题考查了同分异构体数目的求算,题目难度中等,明确同分异构体的书写原则为解答关键,试题侧重考查学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:解答题
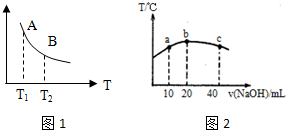
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 自来水的体积 | KI溶液的体积 | 消耗的Na2S2O3溶液的体积 |
| 1 | 10.00mL | 10.00mL | 19.96mL |
| 2 | 10.00mL | 10.00mL | 20.04mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
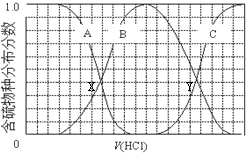
| A. | 含硫物种B表示HS- | |
| B. | 在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为:c(Na+)=3[c(H2S)+c(HS-)+c(S2-)] | |
| C. | X,Y为曲线的两交叉点,若能知道X点处的pH,就可以计算出H2S的Ka值 | |
| D. | NaHS呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是Cu2++HS-═CuS↓+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径A>B>D>C | B. | 原子序数a>b>c>d | ||
| C. | 离子半径D>C>B>A | D. | 金属性B>A,非金属性D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点/K | 沸点/K | 分解温度/K |
| NH3 | 195.3 | 239.7 | 1073 |
| PH3 | 139.2 | 185.4 | 713.2 |
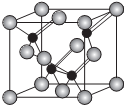
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 2 | 4 | 6 | 8 | 10 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
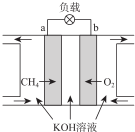
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
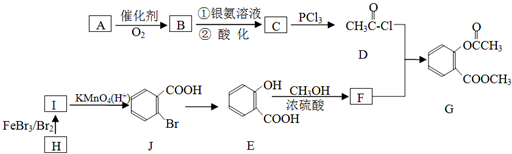
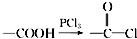 ,请回答以下问题:
,请回答以下问题: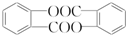 .
.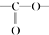 结构
结构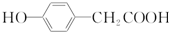 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com