
【题目】X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U的氧化物是第三周期元素形成的常见两性氧化物;W的内层电子全充满,最外层只有1个电子。请回答下列问题:
(1)X、Y、Z的电负性从大到小的顺序是_______ (用元素符号表示,下同)。三种元素的第一电离能由大到小的顺序为__________。
(2)写出Y的价电子排布式____,W同周期的元素中,与W原子最外层电子数相等的元素还有________。
(3)根据等电子体原理,可知化合物XZ的结构式是________, YZ2-的VSEPR模型是________。
(4)X、Y、Z的简单氢化物的键角从大到小的顺序是________ (用化学式表示),原因是_____________。
(5)Y的氢化物易液化的原因是___________。
(6)XZ32-的立体构型是________,其中X原子的杂化轨道类型是________,互为等电子体的离子________。
(7)用氢键表示式写出Z的氢化物中存在的氢键________。
【答案】O>N>C N>O>C 2s22p3 K、Cr C![]() O 平面三角形 CH4>NH3>H2O 价层电子对数相同,孤电子对数越多,斥力越大,键角越小 NH3形成分子间氢键 平面三角形 sp2 NO3- O-H
O 平面三角形 CH4>NH3>H2O 价层电子对数相同,孤电子对数越多,斥力越大,键角越小 NH3形成分子间氢键 平面三角形 sp2 NO3- O-H![]() O
O
【解析】
X、Y、Z、U、W是原子序数依次增大的前四周期元素。其中Y的原子核外有7种运动状态不同的电子,则Y为N元素;U的氧化物是第三周期元素形成的常见两性氧化物,则U为Al;X、Z中未成对电子数均为2,X的原子序数小于N,而Z的原子序数介于N、Al之间,X、Z的核外电子排布分别为1s22s22p2 ,1s22s22p4,故X为C元素、Z为O元素;W的内层电子全充满,最外层只有1个电子,原子序数大于Al,只能处于第四周期,核外电子数为2+8+18+1=29,故W为Cu元素,据此解答。
(1) 周期表中,同周期元素从左到右电负性逐渐增强,则X、Y、Z的电负性从大到小的顺序为O>N>C;同周期随原子序数增大,第一电离能呈增大趋势,但N元素的2p能级为半满的稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能N>O>C,
因此,本题正确答案是:O>N>C ;N>O>C;
(2) Y为N元素,价电子排布式为2s22p3,W为Cu,最外层电子排布为4s1,第四周期中与Cu原子最外层电子数相等的元素还有K、Cr,
因此,本题正确答案是:2s22p3;K、Cr;
(3)根据等电子体原理,可以知道化合物CO与N2互为等电子体,CO的结构式是C![]() O,NO2-的价层电子对数为2+1=3,中心原子的杂化方式为sp2,则VSEPR模型是平面三角形,
O,NO2-的价层电子对数为2+1=3,中心原子的杂化方式为sp2,则VSEPR模型是平面三角形,
因此,本题正确答案是:C![]() O;平面三角形;
O;平面三角形;
(4)X、Y、Z的最简单氢化物分别为CH4、NH3、H2O,3种氢化物的中心原子价层电子对数均为4,VSEPR模型均为正四面体形,但中心原子的孤电子对数依次增大(孤电子对数依次为0、1、2),导致键角变小,故键角:CH4>NH3>H2O,
因此,本题正确答案是:CH4>NH3>H2O;价层电子对数相同,孤电子对数越多,斥力越大,键角越小;
(5) Y的氢化物为氨,是一种易液化的气体,是因为氨分子间存在氢键,分子间作用力大,因而易液化,
因此,本题正确答案是:NH3形成分子间氢键;
(6)CO32-的价层电子对数为3+0=3,没有孤对电子,立体构型是平面三角形,C原子的杂化方式为sp2,与CO32-互为等电子体的离子可以是NO3-,
因此,本题正确答案是:平面三角形;sp2 ;NO3-;
(7)Z为O元素,Z的氢化物为H2O,水分子间存在氢键可表示为O-H![]() O,
O,
因此,本题正确答案是:O-H![]() O。
O。


科目:高中化学 来源: 题型:
【题目】下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
A.漂白粉的成分为次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH溶液处理NO2和HCl废气
D.Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1molH2(g)中的H-H键需要吸收436kJ能量,断裂1molI2(g)中的I-I键需要吸收151kJ能量,生成HI(g)中的1molH-I键能放出299kJ能量。下列说法正确的是
A.1molH2(g)和1molI2(g)的总能量为587kJ
B.H2(g)+I2(s)![]() 2HI(g)ΔH=-11kJ·molˉ1
2HI(g)ΔH=-11kJ·molˉ1
C.HI(g)![]()
![]() H2(g)+
H2(g)+![]() I2(g)ΔH=+5.5kJ·molˉ1
I2(g)ΔH=+5.5kJ·molˉ1
D.H-H键比I-I键更容易断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某气态烃X在标准状况下的密度为1.16g·L-1,A能发生银镜反应,E具有水果香味,有关物质的转化关系。
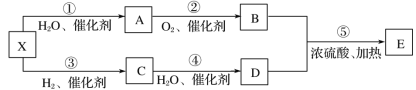
请回答:
(1)C中含有的官能团名称是_________。
(2)化合物M是A的同系物,比A少一个碳原子,请写出M的结构式_________。
(3)下列说法正确的是_________(填字母)。
A.有机物D在加热条件下可以使黑色的氧化铜变红
B.有机物C分子中的所有原子在同一平面上
C.反应③为还原反应,反应④为氧化反应
D.有机物B、D、E均能与NaOH反应
(4)化合物E广泛用于药物、染料、香料等工业,实验室常用如图装置来制备E。装置中,溶液M为_________。反应结束后,将试管中收集到的产品倒入_________中,振荡、静置,然后_________(填操作)分离溶液M。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学生用如图装置研究原电池原理,下列说法错误的是:

A. (3)图中Zn片增重质量与Cu棒减轻质量的比值为65:64
B. (2)图中如果两极上都有气体产生,则说明Zn片不纯
C. (1)图中铜棒上没有气体产生
D. (2)图与(3)图中正极生成物质质量比为1:32时,Zn棒减轻的质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有5种短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)用电子式表示离子化合物A2B的形成过程:______________________。
(2)写出下列物质的电子式: D元素形成的单质__________;E2B________________;A、B、E形成的化合物__________;D、E形成的化合物__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A. ![]()
B. ![]()
C. ![]()
D. ![]() =1000Vρ/(17V+22400)
=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可制成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
①基态镍原子的价电子排布式为________。
②1 mol CH2=CH-CH2OH含___molσ键,烯丙醇分子中碳原子的杂化类型为___。
③Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的分子为_____。
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-中碳与碳之间存在碳碳三键,C22-与O22+互为等电子体,O22+的电子式可表示为_______。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com