
| A、高容量储氢材料的研制是推广应用氢氧燃料电池的关键问题之一 |
| B、发展低碳经济,推广可利用太阳能的城市照明系统有利于节能减排、改善环境质量 |
| C、仅需要托盘天平、砝码、药匙、一定规格的容量瓶、烧杯、玻璃棒这些仪器就可以准确配制出一定浓度的NaCL溶液 |
| D、节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
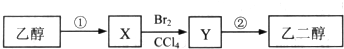
| A、X可以发生加成反应 |
| B、步骤①的反应类型是水解反应 |
| C、步骤②需要在氢氧化钠醇溶液中反应 |
| D、等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10℃时,粉末状锌与2mol?L-1硫酸溶液反应 |
| B、30℃时,粉末状锌与2mol?L-1硫酸溶液反应 |
| C、10℃时,块状锌与2mol?L-1硫酸溶液反应 |
| D、30℃时,块状锌与2mol?L-1硫酸溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲酸能与水以任意比互溶 |
| B、1mol/L甲酸溶液的PH约为2 |
| C、10mL1mol/L甲酸恰好与10mL1mol/LNaOH溶液完全反应 |
| D、在相同条件下,甲酸溶液的导电性比强酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑤ | B、②③⑥ |
| C、①⑤⑥ | D、③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、390.7kj/mol |
| B、-679.3kj/mol |
| C、-787kj/mol |
| D、+180.9kj/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑥ | B、②⑥ | C、①③ | D、①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
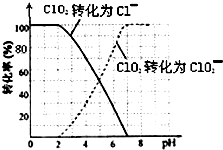 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com