
| A、pH=1的一元酸和pH=13的一元碱等体积混合:c(OH-)=c(H+) |
| B、0.1mol/L的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| C、0.1mol/L的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D、室温下,氢氧化钠与氯化铵的混合溶液中pH=7,则有c(Cl-)=c(NH4+)+c(Na+) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、b-(lga+14) |
| B、3b-(lga+42) |
| C、3b+(lga-42) |
| D、b-(3lga+14) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2O、H2O |
| B、N2、O2、H2O |
| C、N2、HNO3、H2O |
| D、NH3、NO、H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
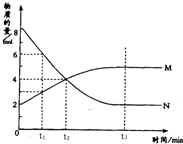 在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为N=2M |
| B、t1时,N的浓度是M浓度的2倍 |
| C、t2时,正逆反应速率相等达到平衡状态 |
| D、t3时,正逆反应速率相等达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、Cl-、I-、Na+ |
| B、NH4+、Al3+、NO3-、Cl- |
| C、Ca2+、K+、Cl-、CO32- |
| D、K+、H+、F-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、④⑦ |
| C、③④⑤ | D、③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- |
| B、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
| C、粗铜精炼时,与电源正极相连的是粗铜,电极反应式仅为:Cu一2e-=Cu2+ |
| D、钢铁无论发生析氢腐蚀,还是吸氧腐蚀,负极反应式都为:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝和氢氧化钠溶液反应:2Al+2OH-→2AlO2-+3H2↑ |
| B、铁和稀盐酸反应:2Fe+6H+→2Fe3++H2↑ |
| C、硫化亚铁溶于稀硝酸中:FeS+2H+→Fe2++H2S↑ |
| D、铁粉和氯化铁溶液反应:Fe+2Fe3+→3Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com