
��1��д����ʵ���з�����Ӧ�Ļ�ѧ����ʽ��
��2����ͨ������ȷ�����ƿ�����Ԫ�ص�����������
(1)��2Na+2H2O==2NaOH+H2![]() ��Na2O+H2O==2NaOH
��Na2O+H2O==2NaOH
��2Al+2NaOH+2H2O==2NaAlO2+3H2![]()
��2��n(Al)=![]() =0.010mol
=0.010mol
���ݷ�Ӧ�ۿɵ���������NaOH�����ʵ���Ϊn(NaOH)=0.010mol���ɵ����������ʵ���Ϊn(H2)=0.015mol��ô�ɽ��������ɵ����������ʵ���Ϊ
n(H2)=![]()
���ݷ�Ӧ�ٿɵý����Ƶ����ʵ���Ϊn(Na)=2��0.035mol=0.070mol����Ϊ��Ӧ����Һ�е�NaOH�����ʵ���Ϊ
n(NaOH)=2.0L��0.050mol��L-1=0.10mol
������Һ��Na+�������ʵ�����ԭ�����Ƶ������ʵ���Ϊ
n(Na+)=0.10mol+0.010mol=0.11mol
n(Na2O)=![]()
���ƿ�����Ԫ�ص���������Ϊ��
![]()
�𣺸��ƿ�����Ԫ�ص���������ԼΪ89%��


 �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д� ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
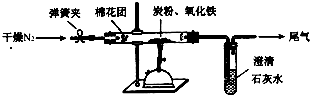 ij�о���ѧϰС��Թ���̿������������Ӧ���������ɷֽ����о���
ij�о���ѧϰС��Թ���̿������������Ӧ���������ɷֽ����о����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ѧ�� | B���������� | C��̫���� | D�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com