
【题目】配平(1)(2);用双线桥法表示(3)(4)氧化还原反应的电子转移。
(1)(_____)KI+(_____)KIO3+(_____)H2SO4—(_____)I2+(_____)K2SO4+(_____)H2O
(2)(_____)Cu2S + (_____)HNO3 — (_____) Cu(NO3)2 + (_____)H2SO4 + (_____)NO2↑+(______)H2O
(3)MnO2+4HCl(浓)![]() MnCl2+C12↑+2H2O______
MnCl2+C12↑+2H2O______
(4)3S+6KOH=K2SO3+2K2S+3H2O_______
【答案】5 1 3 3 3 3 1 14 2 1 10 6 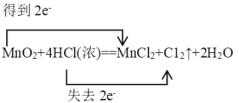

【解析】
首先找出变价的元素,然后结合电子得失守恒和原子守恒分析解答。
(1)碘酸钾作氧化剂,化合价降低5,碘化钾作还原剂,化合价升高1,根据化合价升降守恒(即得失电子守恒),KI的系数为5,碘单质的系数为3,再根据原子守恒进行配平,最终得到方程式为5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O;
(2)硫化亚铜作还原剂,化合价共升高10,硝酸作氧化剂,化合价降低1,根据化合价升降守恒(即得失电子守恒),硫化亚铜的系数为1,硝酸铜的系数为2,硝酸作氧化剂的部分系数为10,又因为2份硝酸铜中N元素没有发生变价,故硝酸的系数为14,根据原子守恒进行剩余部分的配平,最终得到的方程式为Cu2S+14HNO3=2Cu(NO3)2+H2SO4+10NO2↑+6H2O;
(3)二氧化锰作氧化剂,化合价降低2,氯化氢作还原剂,化合价升高2,故可表示为 ;
;
(4)硫单质自身发生氧化还原反应,化合价从0价分别变化到+4价和-2价,则可表示为 。
。


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某同学用托盘天平(配有1g、2g、5g等砝码)称取3.0gNaCl晶体,操作时将药品与砝码的位置放颠倒了,则实际称得的NaCl晶体的质量
A.大于3.0gB.小于30g
C.等于3.0gD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、R、Q原子序数依次增大。由这些元素组成的化合物甲、乙、丙、丁的0.1mol/L水溶液pH如下表,丙、丁为二元化合物。甲溶液逐滴滴入丙溶液中,先产生白色沉淀,后沉淀消失;乙的水溶液可除油污。下列说法一定正确的是

A. W和Q形成的化合物只含有离子键
B. Y和Z的氢化物沸点:Y<Z
C. 离子半径:r(Q>r(R)>r(Z)
D. Y和Q氧化物的水化物酸性:Q>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某生产工艺中用惰性电极电解Na2CO3溶液获得NaHCO3和NaOH,其原理如题21图。下列有关说法正确的是
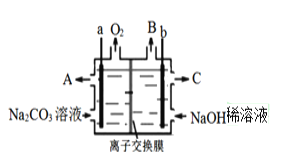
A. a 接外电源负极
B. B出口为H2,C出口为NaHCO3溶液
C. 阳极电极反应为4CO32-+2H2O-4e- = 4HCO3-+O2↑
D. 应选用阳离子交换膜,电解时Na+从右侧往左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种难溶金属硫化物的溶度积常数(25℃):
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10﹣18 | 1.3×10﹣36 | 2.5×10﹣13 |
下列有关说法中正确的是( )
A. 25℃时,CuS的溶解度大于MnS的溶解度
B. 25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10﹣36 molL﹣1
C. 因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生
D. 除去某溶液中的Cu2+,可以选用FeS作沉淀剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验
实验一 | 实验二 | |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写下列空白:
Ⅰ.(1)除去NaCl固体中混有的少量KNO3,所进行的实验操作依次为________、蒸发、结晶、________。
(2)除去KCl溶液中的SO42-,依次加入的溶液为(填溶质的化学式)_____________________。
(3)下列物质的分离和提纯方法操作为①花生油、水混合物________;②碘水中的I2________;
Ⅱ.(1)含有6.02×1023个H的H2O,其物质的量是________;1 mol Na2SO4溶于水能电离出______个Na+、______个SO42-。
(2)______mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.FeCl2溶液中滴加KSCN溶液,溶液不呈血红色
B.K2CO3溶液在火焰上灼烧时,火焰呈蓝色
C.干燥的氯气能使干燥有色布条褪色
D.乙醇可萃取碘水中的碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)高炉炼铁过程中发生的主要反应为
![]()
已知该反应在不同温度下的平衡常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(C02)= _____________、CO的平衡转化率= _____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
A.减少Fe的量 | B.增加Fe203的量 | C.移出部分C02 |
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com