
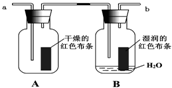
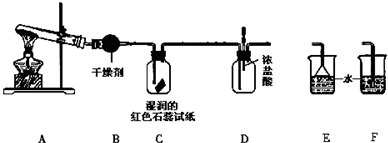
 为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答:
为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答:分析 (1)如从b通入,则进入A的氯气将不再干燥;
(2)集气瓶A中干燥的红色布条不褪色,说明氯气不具有漂白性;
(3)集气瓶B中湿润的红色布条褪色,说明次氯酸具有漂白性.
解答 解:(1)如从b通入,则进入A的氯气将不再干燥,则A中的干燥红色布条也会褪色,因此实验时,将干燥的氯气从a通入,
故答案为:a;
(2)集气瓶A中干燥的红色布条不褪色,说明氯气不具有漂白性,红色布条褪色的原因与氯气无关,
故答案为:干燥的红色布条不褪色,说明与氯气无关;
(3)集气瓶B中湿润的红色布条褪色,说明氯气与水反应生成次氯酸,次氯酸使红色布条褪色,次氯酸具有漂白性,
故答案为:湿润的红色布条褪色,说明氯气与水反应生成次氯酸,次氯酸使红色布条褪色.
点评 本题考查氯气的性质,题目难度不大,本题注意氯气使有色布条褪色的原因是能生成具有漂白性的HClO.


科目:高中化学 来源: 题型:选择题
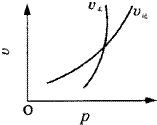 符合图象的反应为( )
符合图象的反应为( )| A. | N2O3(g)?NO2(g)+NO(g) | B. | 3NO2(g)+H2O (l)?2HNO3(l)+NO(g) | ||
| C. | 4NO2(g)+5O2 (g)?4NO(g)+6H2O(g) | D. | CO2(g)+C(s)?2CO(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
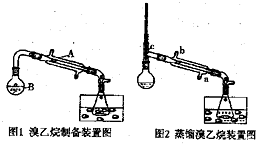 已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:| 溶解性(本身均做溶剂) | 沸点(℃) | 密度(g/mL) | |
| 水混溶,易溶于有机溶剂 | 78.5 | 0.8 | |
| 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
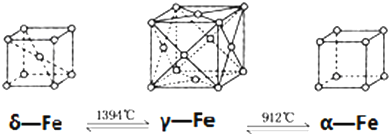
| A. | δ、γ、α三种晶体互为同分异形体 | |
| B. | α-Fe晶体中与每个铁原子等距离且最近的铁原子有6个 | |
| C. | 将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型不同,化学性质相同 | |
| D. | γ-Fe晶体为面心立方密堆积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com