
【题目】为了实现资源利用最大化,某化工厂将合成氨、制纯碱和生产尿素![]() 工艺联合,简易流程如下:
工艺联合,简易流程如下:

![]() 时101kPa时,测得生成17g
时101kPa时,测得生成17g![]() ,放出
,放出![]() 热量,写出合成
热量,写出合成![]() 的热化学方程式 ______ .
的热化学方程式 ______ .
![]() 合成氨原料气中的杂质硫化氢用稀氨水吸收,副产品是酸式盐.该副产品的化学式为 ______ .
合成氨原料气中的杂质硫化氢用稀氨水吸收,副产品是酸式盐.该副产品的化学式为 ______ .
![]() 反应器2分离出来的氮气和氢气再通入反应器1,其目的是 ______
反应器2分离出来的氮气和氢气再通入反应器1,其目的是 ______ ![]() 向反应器3充入原料的顺序是:先加氯化钠溶液,通入氨气至饱和,再通入足量的二氧化碳可制得
向反应器3充入原料的顺序是:先加氯化钠溶液,通入氨气至饱和,再通入足量的二氧化碳可制得![]() 反应器3中的化学方程式为 ______ .
反应器3中的化学方程式为 ______ .
![]() 工业上可用碳、甲烷与水蒸汽反应制氢气
工业上可用碳、甲烷与水蒸汽反应制氢气
![]() ,
,![]() ,此反应的化学平衡常数表达式为
,此反应的化学平衡常数表达式为![]() ______ ,为了提高碳的转化率,宜采用下列措施中的
______ ,为了提高碳的转化率,宜采用下列措施中的![]() 填字母编号
填字母编号![]() ______ .
______ .
A.增大压强![]() 增加碳的量
增加碳的量![]() 升高温度
升高温度![]() 增加水的量
增加水的量![]() 使用催化剂
使用催化剂![]() 及时移出CO、
及时移出CO、![]()
![]() 有些国家水电丰富,采用惰性电极电解硫酸钠溶液制氢气,电解时阳极上的电极反应式为 ______
有些国家水电丰富,采用惰性电极电解硫酸钠溶液制氢气,电解时阳极上的电极反应式为 ______
![]() 若仅以
若仅以![]() 、空气、
、空气、![]() 为原料制尿素
为原料制尿素 ,标准状况下
,标准状况下![]()
![]() ,理论上最多能制 ______
,理论上最多能制 ______ ![]() 尿素.
尿素.
【答案】![]()
![]() 提高原料利用率
提高原料利用率 ![]()
![]() CDF
CDF ![]() 60
60
【解析】
![]() 和
和![]() 完全反应生成17g即
完全反应生成17g即![]() 放热
放热![]() 热量,生成2mol氨气放热
热量,生成2mol氨气放热![]() ,反应为放热反应,反应的焓变为
,反应为放热反应,反应的焓变为![]() ,依据热化学方程式书写得到;
,依据热化学方程式书写得到;
![]() 硫化氢与氨水反应生成
硫化氢与氨水反应生成![]() ;
;
![]() 氮气和氢气再通入反应器1可节约燃料;氯化钠、氨气和二氧化碳可反应生成碳酸氢钠和氯化铵;
氮气和氢气再通入反应器1可节约燃料;氯化钠、氨气和二氧化碳可反应生成碳酸氢钠和氯化铵;
![]() 平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积;为提高某一反应物的转化率,应使平衡向正反应反应方向移动;
平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积;为提高某一反应物的转化率,应使平衡向正反应反应方向移动;
![]() 电解硫酸钠溶液实质是电解水;
电解硫酸钠溶液实质是电解水;
![]() 由C原子守恒可知,
由C原子守恒可知,![]() ,以此计算.
,以此计算.
![]() 和
和![]() 完全反应生成17g即
完全反应生成17g即![]() 放热
放热![]() 热量,生成2mol氨气放热
热量,生成2mol氨气放热![]() ,反应为放热反应,反应的焓变为
,反应为放热反应,反应的焓变为![]() ,反应的热化学方程式为:
,反应的热化学方程式为:![]() ;
;
故答案为:![]() ;
;
![]() 硫化氢与氨水反应生成
硫化氢与氨水反应生成![]() ,故答案为:
,故答案为:![]() ;
;
![]() 氮气和氢气再通入反应器1可节约燃料,提高原料利用率;氯化钠、氨气和二氧化碳可反应生成碳酸氢钠和氯化铵:
氮气和氢气再通入反应器1可节约燃料,提高原料利用率;氯化钠、氨气和二氧化碳可反应生成碳酸氢钠和氯化铵:![]() ,
,
故答案为:提高原料利用率;![]() ;
;
![]() 平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积积,所以
平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积积,所以![]() ;为提高碳的转化率,应是反应向正反应方向移动,则可采取的措施有:升高温度、增加水的量、及时分离出CO、
;为提高碳的转化率,应是反应向正反应方向移动,则可采取的措施有:升高温度、增加水的量、及时分离出CO、![]() ,
,
故答案为:![]() ;CDF;
;CDF;
![]() 电解硫酸钠溶液实质是电解水,阳极反应式为
电解硫酸钠溶液实质是电解水,阳极反应式为![]() ,故答案为:
,故答案为:![]() ;
;
![]() 的物质的量是1000mol,由C原子守恒可知,
的物质的量是1000mol,由C原子守恒可知,![]() ,
,![]() 的物质的量是1000mol,质量60000g,即60kg,故答案为:60.
的物质的量是1000mol,质量60000g,即60kg,故答案为:60.


科目:高中化学 来源: 题型:
【题目】MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示,下列叙述中正确的是
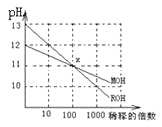
A.MOH和ROH都是强碱
B.在x点,c(M+)=c(R+)
C.稀释前,c(ROH)=10c(MOH)
D.常温下,pH之和为14的醋酸和ROH溶液等体积混合,所得溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与新冠肺炎防疫和检测有关的过程中,没有发生化学反应的是( )
A | B | C | D |
|
|
|
|
以丙烯为原料制备熔喷聚丙烯,作为医用外科口罩的材料 | 电解饱和食盐水制备消毒液,对公共场所进行消毒 | 使用明矾作为絮凝剂,对采集水样进行前处理 | 使用液氨作为制冷剂, 对疫苗进行低温保存 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镍(NiSO4)是一种重要的化工原料,广泛应用于电镀、医药、印染等工业。以含镍废催化剂(主要含Ni及少量的Al、Al2O3、Fe和其它不溶于酸、碱的杂质)为原料生产NiSO4·7H2O晶体的两种工艺流程如下:
流程一:
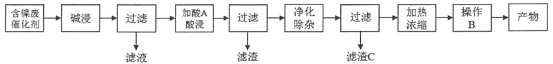
流程二:

已知:部分金属氢氧化物的Ksp近似值如下表所示:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
回答下列问题:
(1)流程一中所用酸A和流程二中所用酸X___________(填“相同”或“不相同”);流程一中滤渣C和流程二中滤渣II___________(填“相同”或“不相同”)。流程二中滤渣I是___________。
(2)流程一中“碱浸”时发生反应的离子方程式为_________________、___________________。
(3)流程二中“净化除杂”包含了两步操作过程:第一步,加入氧化剂H2O2,发生反应的离子方程式是____________________________________________;第二步,调节溶液的pH。
(4)分析比较流程一中操作B和流程二中操作Y后,回答操作Y是___________、___________、过滤、洗涤、干燥,即得产物。
(5)由己知信息列式计算:常温下,Ni2+完全沉淀时的pH值___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是化学学习中非常重要的内容,根据下面两个实验回答问题。
(一)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
试管编号 | 加入试剂 | 实验现象 |
Ⅰ | 2滴0.1mol/LFeCl3溶液 | ①_____ |
Ⅱ | 4mL2mol/LNH4Cl溶液 | ②_____ |
A.白色沉淀转化为红褐色沉淀 B.白色沉淀不发生改变
C.红褐色沉淀转化为白色沉淀 D.白色沉淀溶解,得无色溶液
(2)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:____________________________________________________________。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是____(填 “1”或“2”)。
(二)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.000 0 g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI===3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250 mL,然后取25.00 mL用5.0×10-4 mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O32-===2I-+S4O62-)。有关实验数值如下表所示。
滴定次数 | 待测液的体积(mL) | 滴定前的读数(mL) | 滴定后的读数(mL) |
第一次 | 25.00 | 0.00 | 15.90 |
第二次 | 25.00 | 0.00 | 14.99 |
第三次 | 25.00 | 0.00 | 15.01 |
该碘盐中碘元素的百分含量为________。(保留三位有效数字)下列操作中,会导致所测得的碘元素的百分含量偏大的是________。
a.滴定终时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、杀菌、脱色、除臭的新型高效水处理剂,工业上可通过 Fe(NO3)3 与NaClO在强碱性介质中反应生成紫红色高铁酸盐溶液,其对应的工业流程如图所示。有关说法正确的是( )
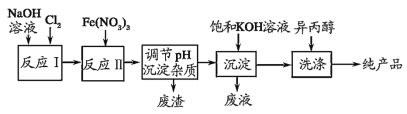
A.K2FeO4能够作为净水剂的原因,在于其氧化产物能够水解生成氢氧化铁胶体
B.反应II的离子方程式为 3ClO+5H2O+2Fe3+=2![]() +3Cl+10H+
+3Cl+10H+
C.向Na2FeO4 中加入饱和KOH 溶液,析出K2FeO4 沉淀,说明K2FeO4 的溶解度比Na2FeO4 大
D.洗涤粗品时选用异丙醇而不用水,可以减少K2FeO4的溶解损失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,原理如图所示,淡水最终在X和Z室中流出。下列说法不正确的是
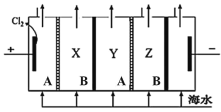
A.一般海水中含有的 Ca2+、Mg2+容易生成沉淀堵塞离子交换膜,因此不能直接通入阴极室
B.阳极发生电极反应:2Cl2e=Cl2↑
C.电渗析过程中阴极附近pH值升高
D.A膜为阳离子交换膜,B膜为阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在定温定容的密闭容器中合成 ![]() 。下列不能说明反应
。下列不能说明反应 ![]() 达到化学平衡状态的是
达到化学平衡状态的是
A.![]() B.容器内的压强不再改变
B.容器内的压强不再改变
C.![]() 的生成速率与
的生成速率与 ![]() 的消耗速率相等D.
的消耗速率相等D.![]() 的转化率不再改变
的转化率不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可通过甲醇羰基化法制取甲酸甲酯(HCOOCH3):CH3OH(g)+ CO(g)=HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如右图所示。下列说法不正确的是
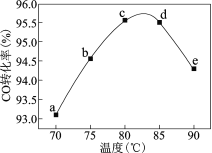
A.增大压强甲醇转化率增大
B.b点反应速率υ正 = υ逆
C.平衡常数K(75℃)>K(85℃),反应速率υb<υd
D.生产时反应温度控制在80~85℃为宜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com