
| A. | CuSO4 | B. | KCl | C. | H2SO4 | D. | Na2SO4 |
分析 用惰性电极电解电解质溶液,阴极的放电顺序:银离子>铜离子>氢离子>钠离子,阳极离子的放电顺序:氯离子>氢氧根离子>硫酸根(硝酸根)离子,根据两个电极的放电顺序,分析电解后溶液的成分来确定pH的变化.
解答 解:A.电解CuSO4溶液时,阳极生成氧气、阴极生成铜,反应后生成有硫酸生成,溶液的pH<7;
B.电解KCl溶液时,阳极上氯离子放电、阴极上氢离子放电,导致溶液中氢氧根离子浓度增大,溶液的pH>7;
C.电解硫酸时,生成氢气和氧气,实质为电解水,酸的浓度升高,溶液的pH最小;
D.电解硫酸钠溶液,实质为电解水,溶液的pH不变,仍然为7;
根据分析可知,电解后A、C、D溶液呈酸性,只有B为碱性,所以溶液pH最大的为B,
故选B.
点评 本题考查了电解原理、溶液pH的大小比较,题目难度中等,明确电解原理为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及灵活应用基础知识的能力.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:推断题
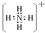 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| C. | 常温常压下,14 g由N2与CO组成的混合气体中含有的原子数目为NA | |
| D. | 标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
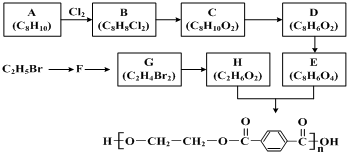
 ;
; (写出结构简式).
(写出结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2C=O+HCN→(CH3)2C(OH)CN | B. | CH3CH2OH→CH2=CH2↑+H2O | ||
| C. | 2CH3CHO+O2→2CH3COOH | D. | CHCl3+HF→CHFCl2+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,新戊烷的结构简式为C(CH3)4.
,新戊烷的结构简式为C(CH3)4.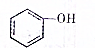 (填“>”、“<”或“=”,下同)
(填“>”、“<”或“=”,下同)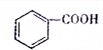 (提示:类比醇与酚的酸性)
(提示:类比醇与酚的酸性) .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ③
③ ⑤
⑤ .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
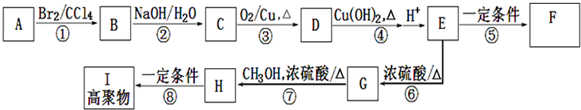
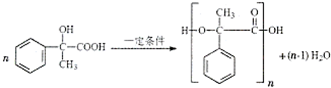
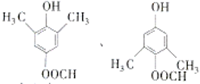
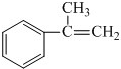 ;E在一定条件下能形成3个六元环的物质,该物质的结构简式为:
;E在一定条件下能形成3个六元环的物质,该物质的结构简式为: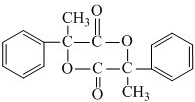 .
.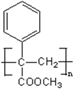 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
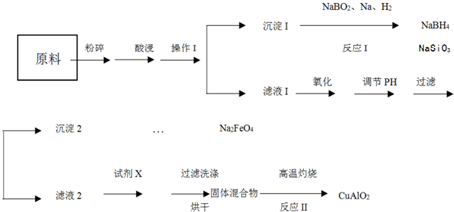
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com