
【题目】H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
(1)定性分析:图甲可通过观察_______________________________________定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_____________________________。
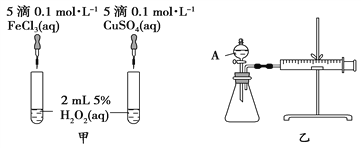
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看__________________________,实验中需要测量的数据是____________________________________________________。
(3)课本在研究浓度对反应速率影响的实验中,酸性高锰酸钾和弱酸草酸反应的离子方程式为____________________________________________________,反应开始一段时间后反应速率明显提升的原因是_________________________________________________________________。
【答案】 产生气泡的快慢 阴离子相同更能说明铁离子和铜离子的催化效果 注射器活塞是否复原 生成40mL气体所需要的时间 5H2C2O4十2MnO4--+6H+ = 2Mn2+十10CO2↑十8H2O 反应生成锰离子起催化作用
【解析】(1)该反应中产生气体,可根据生成气泡的快慢判断,氯化铁和硫酸铜中阴阳离子都不同,无法判断是阴离子起作用还是阳离子起作用,硫酸铁和硫酸铜阴离子相同,可以消除阴离子不同对实验的干扰;
(2)结合乙图装置,该气密性的检查方法为:关闭分液漏斗活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;反应是通过反应速率分析的,根据v=![]() ,所以,实验中需要测量的数据是时间(或收集一定体积的气体所需要的时间);
,所以,实验中需要测量的数据是时间(或收集一定体积的气体所需要的时间);
(3)酸性高锰酸钾溶液具有强氧化性,能氧化草酸根离子生成二氧化碳,同时自身被还原生成二价锰离子,离子反应方程式为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O,反应速率提升的原因可能是反应中生成的Mn2+对该反应有催化效果。


科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海洋植物中提取碘的流程如下: ![]()
某化学兴趣小组将上述流程②③设计成如图所示实验.
已知:②中发生反应的化学方程式为Cl2+2KI═2KCl+I2 .
(1)写出提取流程中①③实验操作的名称:① , ③ .
(2)四氯化碳是无色、密度比水大的液体.F中下层液体的颜色为色,上层液体中溶质的主要成分为 .
(3)从F中得到碘单质还需进行的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质按酸、碱、盐分类排列,正确的是
A. 硝酸、生石灰、石灰石 B. 醋酸、纯碱、食盐
C. 盐酸、乙醇、硝酸钾 D. 硫酸、烧碱、碳酸氢钠
查看答案和解析>>
科目:高中化学 来源: 题型:
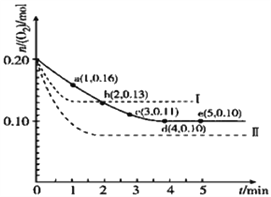
【题目】一定温度下,在2L的密闭容器中充入0.4mol SO2和0.2mol O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g)△H<0,n(O2)随时间的变化关系如图实线所示:
2SO3(g)△H<0,n(O2)随时间的变化关系如图实线所示:
(1)该温度下反应的平衡常数K为_______________(不用带单位),升高温度K值将_______________(填增大、不变或减小,下同)。
(2)若温度不变,在容器中再加1mol O2,重新达到平衡,则SO2的平衡浓度将_______________,氧气的转化率将_______________,SO3的体积分数将_______________。
(3)仅改变某一实验条件再进行两次实验,测得O2的物质的量随时间变化如图中虚线所示,曲线Ⅰ改变的实验条件是_______________,曲线Ⅱ改变的实验条件是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中正确的是( )
A.HF溶于少量水中:HF+H2OF﹣+H3O+
B.H2S溶于水:H2S2H++S2﹣
C.Na2HPO4溶于水:Na2HPO4═2Na++H++PO43﹣
D.NaHSO4熔融:NaHSO4═Na++H++SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用480mL、0.5mol/L 的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为
(2)将下列步骤中的空格内所用仪器补充填写完整 ①用20mL量筒量取所需的浓硫酸
②将烧杯中的溶液转移到mL的容量瓶中
③将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
④将溶液冷却,恢复至室温
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦洗涤烧杯2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀.
(3)实验中上述步骤的正确顺序为(填序号).
(4)填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”). ①所用的浓硫酸长时间放置在密封不好的容器中
②量取浓硫酸所用量筒有蒸馏水
③定容时,俯视液面
(5)取用任意体积的所配0.5mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是(填字母)
A.溶液中H2SO4的物质的量
B.溶液的浓度
C.溶液中SO42﹣的数目
D.溶液的密度
(6)在容量瓶上,下列标记不存在的是(填字母)
A.标线
B.温度
C.浓度
D.容量规格.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下将44.8LHCl气体溶于1L水中,所得盐酸溶液的密度为1.1g/cm3,该盐酸的物质的量浓度为
A. 2mol/L B. 2.1mol/L C. 2.2mol/L D. 2.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在容积为2L的3个恒容密闭容器中发生反应:3A(g)+B(g)![]() xC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
xC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物的投入量 | 3molA、2molB | 6molA、4molB | 2molC |
还到平衡的时间/min | 5 | 8 | |
A的浓度/mol L-1 | cl | c2 | O |
C的体积分数/% | ω1 | ω3 | |
混合气体的密度/g·L-1 | ρ1 | ρ2 |
下列说法正确的是
A. 若x<4,则2c1<c2
B. 若x=4,则ω1=ω3
C. 无论x的值是多少,均有2ρ1=ρ2内
D. 容器甲中反应从开始到平衡的平均反应速率可能为v(A)=0.3mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com