
| A、碳酸钠溶液和稀盐酸 |
| B、偏铝酸钾溶液和稀硫酸 |
| C、硫酸铝溶液和氨水 |
| D、氯化铝溶液和氢氧化钡溶液 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、c(CH3COOH)>c(CH3COO-) |
| B、c(Na+)+c(H+)=c(CH3COO-)+c(CH3COOH)+c(OH-) |
| C、c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D、c(CH3COO-)+c(CH3COOH)=0.02 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
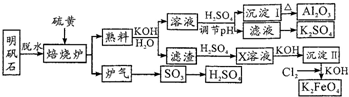
 铁是人类应用较早,当前应用量最大的金属元素.
铁是人类应用较早,当前应用量最大的金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:
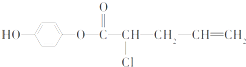 ,下列叙述中,正确的是( )
,下列叙述中,正确的是( )| A、该有机物的分子式为C11H13O3Cl |
| B、1mol该有机物最多可消耗2molNaOH |
| C、该有机物既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色 |
| D、该有机物中所有原子一定在同一平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Ca2+、Na+、CO32- |
| B、Mg2+、Al3+、SO42-、Cl- |
| C、Cu2+、Mg2+、Cl-、OH- |
| D、K+、Na+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、向稀Fe(NO3)2和NaBr混合溶液中滴加稀盐酸6Br-+8H++2NO3-=3Br2+2NO↑+4H2O |
| C、Na2S溶液中滴加NaClO溶液:S2-+ClO-+H2O=S↓+Cl-+2OH- |
| D、双氧水使酸性KMnO4溶液褪色2MnO4-+5H2O2=2Mn2++5O2↑+6OH-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①和② | B、②和③ |
| C、③和④ | D、④和⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com