
| A. |  | B. |  | C. |  | D. |  |
科目:高中化学 来源: 题型:解答题
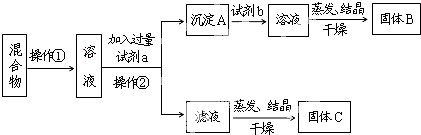
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 若a=b,则混合后溶液中一定有:c(X-)=c(Y+)>c(H+)=c(OH-) | |
| B. | 若m+n=14,则混合后溶液一定显中性 | |
| C. | 若混合后溶液中c(X-)<c(Y+),则该混合溶液一定显碱性 | |
| D. | 若a=b,混合后溶液pH<7,则一定生成强酸弱碱盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢镁溶液中加入足量的烧碱:HCO3-+OH-=CO32-+H2O | |
| B. | 铝粉投入到烧碱溶液中:Al+2OH-=AlO2-+H2↑ | |
| C. | 铁粉加到足量的稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 向FeSO4和KSCN溶液滴加酸化的H2O2溶液,立即变红:2Fe2++H2O2+2H+=2Fe3++2H2O,Fe3++3SCN-=Fe(SCN)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
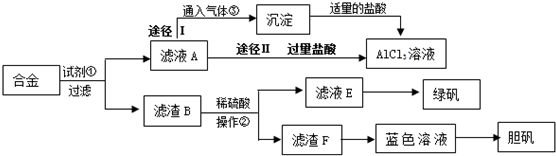
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如表所示:(已知果汁是显酸性的)
某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如表所示:(已知果汁是显酸性的)| 实验编号 | 水果种类 | 电极间距离 | 电流大小/μA |
| ① | 西红柿 | 1 | 98.7 |
| ② | 西红柿 | 2 | 72.5 |
| ③ | 苹果 | 2 | 27.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;N2的电子式
;N2的电子式 ;
;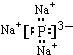 ,其中的化学键为离子键.
,其中的化学键为离子键.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
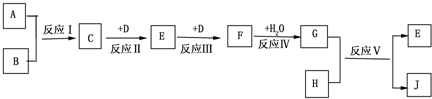
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com