
A、 |
| B、HCO3- |
| C、HSO4- |
D、 |
 是Al3+,是弱碱阳离子,能结合水电离出的OH-,使水的电离平衡右移,溶液显酸性,故A错误;
是Al3+,是弱碱阳离子,能结合水电离出的OH-,使水的电离平衡右移,溶液显酸性,故A错误; 是F-,是弱酸根,能结合水电离出的H+而水解,故对水的电离有促进作用,但使溶液显碱性,故D正确.
是F-,是弱酸根,能结合水电离出的H+而水解,故对水的电离有促进作用,但使溶液显碱性,故D正确.

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:
| A、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B、26g乙炔所含共用电子对数目为2NA |
| C、标准状况下,11.2L CCl4所含分子数为0.5NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
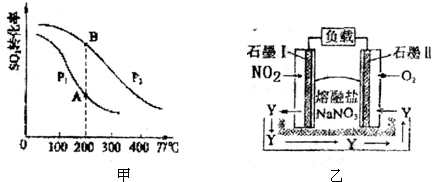
| ||
| 高温 |
| 气体 | SO2 | O2 | SO3 |
| 物质的量(mol) | 1.6 | 1.8 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
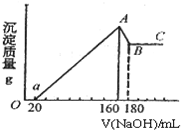 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1NaOH 溶液:K+、Na+、SO42-、CO32- |
| B、0.1mol?L-1Na2CO3 溶液:Al3+、Ba2+、NO3-、Cl- |
| C、0.1mol?L-1FeCl3 溶液:K+、NH4+、I-、SCN- |
| D、由水电离的c(H+)=1.0×10-9 mol?L-1溶液:Ca2+、Na+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④③②① | B、①④③② |
| C、②③④① | D、①④②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C |
| B、C和S |
| C、KNO3 |
| D、S和KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 1.2 mol?L-1的NaCl溶液 |
| B、2 L 1 mol?L-1的NaOH溶液 |
| C、0.5 L 0.8 mol?L-1的Na2SO4溶液 |
| D、3 L 0.5 mol?L-1的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10mL 0.5mol/L的明矾溶液与10mL0.5mol/LBa(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓ | ||||
| B、硫酸铜溶液显酸性:Cu2++2H2O═Cu(OH)2↓+2H+ | ||||
C、向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-
| ||||
| D、用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com