
| A.新型无机非金属材料具有光学特性、生物功能、电学特性、耐高温、强度高 |
| B.光导纤维做通讯材料有许多优点,但怕腐蚀,铺设也很不方便 |
| C.高温结构陶瓷比金属材料具有许多优点,如不怕氧化、密度小等优点 |
| D.光导纤维除用于通信外,还可以用于医疗、信息处理等许多方面 |
科目:高中化学 来源:不详 题型:单选题
| A.单质硅可用于制造光纤和太阳能电池 |
| B.在常温下可用铝制容器贮藏运输浓硫酸 |
| C.纯碱可作治疗胃酸过多的一种药剂 |
| D.SO2可用于漂白一切有色物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SiO2(制光纤) | B.Si和Ge(半导体材料) |
| C.钢化玻璃(汽车窗玻璃) | D.氮化硅陶瓷(制导热剂) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SiO2具有导电性,可用于制造半导体材料 |
| B.Cl2能与石灰乳反应,可用于制取漂白粉 |
| C.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿 |
| D.常温下浓H2SO4能使铁发生钝化,可在常温下用铁制容器贮运浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 1 |
| 2 |
| 容器编号 | c(CO)/mol?L-1 | c(O2)mol?L-1 | c(CO2)mol?L-1 | v(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正)______v(逆) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制备粗硅不涉及氧化还原反应 |
| B.光导纤维的主要成份是二氧化硅 |
| C.二氧化硅是H2SiO3的酸酐,因此能与水反应,也能与碱溶液反应 |
| D.常温时硅既能与盐酸反应,也能与烧碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇与乙酸的酯化反应 | B.甲烷与氧气的反应 |
| C.铁与氯气的反应 | D.次氯酸的分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
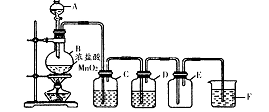
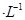 的溶液缓缓通入100 mLCl2(标准状况),溶液由浅绿色逐渐变黄色;继续通人Cl2,溶液黄色加深,变为棕黄色。
的溶液缓缓通入100 mLCl2(标准状况),溶液由浅绿色逐渐变黄色;继续通人Cl2,溶液黄色加深,变为棕黄色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com