

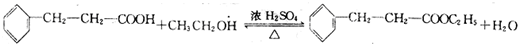 .
.
 .
. 分析 (1)根据A的结构简式可知A的分子式;
(2)根据D的结构简式可知其中含氧的官能团;
(3)含有醛基官能团的能发生银镜反应;
(4)C经一步反应可生成E,E是B的同分异构体,E能发生酯化反应得F,根F的分子式结合B的结构简式可知,E为羧酸,E为C6H5CH2CH2COOH,F为 ,反应①为氧化反应,反应②为酯化反应;
,反应①为氧化反应,反应②为酯化反应;
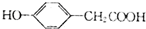
(5)化合物G为D的同分异构体,G为对位二取代苯结构,且G能与FeCl3溶液发生显色反应,说明G中有酚羟基,G还能与NaHCO3溶液反应放出CO2气体,说明G中有羧基,据此写出G的结构简式.
解答 解(1)根据A的结构简式可知A的分子式为C11H12O2,
故答案为:C11H12O2;
(2)根据D的结构简式可知其中含氧的官能团为羧基和羟基,
故答案为:羧基和羟基;
(3)含有醛基官能团的能发生银镜反应,A、C中都含有醛基,
故选A、C;
(4)C经一步反应可生成E,E是B的同分异构体,E能发生酯化反应得F,根F的分子式结合B的结构简式可知,E为羧酸,E为C6H5CH2CH2COOH,F为 ,反应①为氧化反应,反应②为酯化反应,反应②的化学方程式为
,反应①为氧化反应,反应②为酯化反应,反应②的化学方程式为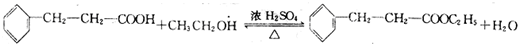 ,
,
故答案为:氧化反应;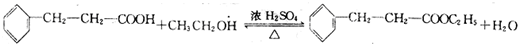 ;
;
(5)化合物G为D的同分异构体,G为对位二取代苯结构,且G能与FeCl3溶液发生显色反应,说明G中有酚羟基,G还能与NaHCO3溶液反应放出CO2气体,说明G中有羧基,则符合条件的G的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的结构和性质,为高频考点,明确有机物的官能团与性质的关系即可解答,并注意利用同分异构体、酯化反应的特点来解答,题目难度中等.


科目:高中化学 来源: 题型:解答题
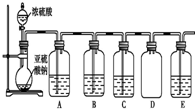 (1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.
(1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.| 物质 | 类别 | 化学性 质预测 | 实验验证 | ||
| 实验操作 | 实验现象 | 实质(用离子 方程式表示) | |||
| 二氧 化硫 | 酸性 氧化物 | 与水 反应 | 将盛满SO2气体的试管倒立在水中,并测定试管中溶液的pH | ① | SO2+H2O ?H2SO3 |
| 与碱 反应 | ② | 出现白 色沉淀 | ③ | ||
| 装置 | 药品 | 作用 |
| A | 验证二氧化硫的还原性 | |
| B | ||
| C | 品红溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有金属元素 | |
| B. | 只由共价键构成的物质不一定是共价化合物 | |
| C. | 原煤、天然气属于一次能源,而电力、蒸汽则属于二次能源 | |
| D. | 锌锰电池是一次电池,而铅蓄电池则是二次电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
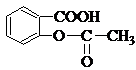 转变为
转变为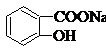 的方法是( )
的方法是( )| A. | ①② | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
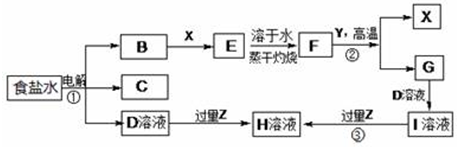
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加催化剂同时增大压强 | B. | 加催化剂同时升高温度 | ||
| C. | 升高温度同时充入CO2 | D. | 降低温度同时降低压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2 | B. | HCl | C. | Ba(OH)2 | D. | NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com