
用右图表示的一些物质或概念之间的从属或包含关系中不正确的是
| X | Y |
| |||
| A | 盐 | 化合物 | 纯净物 | ||
| B | 溶液 | 分散系 | 混合物 | ||
| C | 强电解质 | 电解质 | 化合物 | ||
| D | 氧化物 | 酸性氧化物 | 碱性氧化物 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
键能是指破坏(或形成)1mol化学键所吸收(或放出)的能量。现查得:H-H、Cl-Cl和H-Cl的键能分别为436kJ/mol、243kJ/mol和431kJ/mol,请用此数据估计,由Cl2、H2生成1molHCl时的热效应为( )
A.放热91.5kJ B.放热183kJ C.吸热183kJ D.吸热91.5kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到目的的是 (  )。
)。
A.将铜丝插入浓硫 酸中加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色
酸中加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿
查看答案和解析>>
科目:高中化学 来源: 题型:
在工业中利用镁制取硅:2Mg+SiO2 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:

(1)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通入X气体,再加热反应物,其理由是______________,
当反应开始后,移走酒精灯反应能继续进行,其原因是___________。
(3)反应结束后,待冷却至常温时 ,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原因用化学方程式表示
,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原因用化学方程式表示 为_______________。
为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列物质分类全部正确的是
①生石灰 ②食盐 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
A.碱—①④ B.纯净物—③④⑤ C.盐—②⑥ D.混合物—③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶 液; ③ 加入稍过量的BaCl2 溶液;④滴入适量的稀盐酸;⑤ 过滤。正确的操作顺序是
A.②③①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合溶液中所含离子的浓度如下表,则M离子可能为
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度/(mol·L-1) | 1 | 1 | 2 | 1 |
A.Na+ B.Ba2+ C.F- D.S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D是中学化学中常见的四种不同微粒。它们之间存在如下图所示的关系:
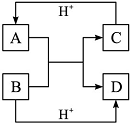
(1)如果A、B、C、D均为10电子的微粒,且C的水溶液呈碱性,请写出A的结构式:
________________________________________________________________________。
(2)如果A和C是18电子微粒,B和D是10电子微粒,请写出:
①A与B在溶液中反应的离子方程式:__________________________________________
________________________________________________________________________。
②根据上述离子方程式,可以判断C与B结合质子的能力大小是:________>________。(用化学式或离子符号表示)
③已知肼(H2N—NH2)和甲胺(CH3—NH2)都是含有18个电子的分子。分析肼和甲 胺的结构特点并从中受到启发,写出与其具有相同电子数的有机化合物的结构简式(至少写两个):
胺的结构特点并从中受到启发,写出与其具有相同电子数的有机化合物的结构简式(至少写两个):
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)相同质量的SO2气体和SO3气体,其分子数之比为________,氧原子数之比为________,相同条件下(同温同压)的体积之比为________,密度之比为________。
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是________,这种混合气体的密度是同温同压下氧气密度的________倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com