
【题目】下列物质与水反应会放出氧气的是
A. Na2O B. Na2O2 C. K D. NO2
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】Fe与水蒸气反应实验装置如图所示。
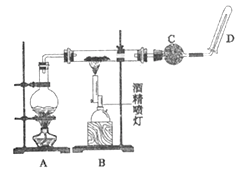
(1)装置A的作用是_________。
(2)B中反应的化学方程式为_____。
(3)C的作用是除杂,使用的试剂是_________。
(4)在D处玻璃管口点燃生成的气体前,必须对该气体进行_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示,电解槽内装有 KI 及淀粉溶液,中间用阴离子交换膜 隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变 浅。已知:3I2+6OH﹣=IO3﹣+5I﹣+3H2O,下列说法不正确的是( )
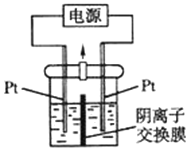
A. 右侧发生的电极反应式:2H2O+2e﹣=H2↑+2OH﹣
B. 电解结束后,右侧溶液中含有 IO3﹣
C. 电解槽内发生反应的总化学方程式:KI+3H2O![]() KIO3+3H2↑
KIO3+3H2↑
D. 如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚丙烯酸钠(![]() )具有超强吸水性,能吸收空气中的水分,可用于矿 山道路运输抑尘等。下列叙述不正确的是( )
)具有超强吸水性,能吸收空气中的水分,可用于矿 山道路运输抑尘等。下列叙述不正确的是( )
A. 聚丙烯酸钠属于纯净物 B. 聚丙烯酸钠可用于生产尿不湿
C. 聚丙烯酸钠的单体为CH2=CH—COONa D. 路面喷洒聚丙烯酸钠溶液能抑制扬尘,一定程度上能预防雾霾和 PM2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中发生反应的离子方程式为:Zn+2H+→Zn2++H2↑,下列说法错误的是( )

A. 该装置可能是原电池,电解质溶液为稀盐酸
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. a、b 不可能是同种材料的电极
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2FeO4是一种高效多功能水处理剂,应用前景广阔,一种制备Na2FeO4的方法如下:![]() ,对此反应下列说法错误的是
,对此反应下列说法错误的是
A. Na2O2在反应中既是氧化剂也是还原剂
B. 1 mol FeSO4发生反应时,共有4mol电子转移
C. Na2FeO4既是氧化产物又是还原产物
D. O2是氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)某有机物的结构简式为: ,该有机物中含氧官能团有:______、______、________、______(写官能团名称)。
,该有机物中含氧官能团有:______、______、________、______(写官能团名称)。
(2)有机物![]() 的系统名称是_____,将其在催化剂存在 下完全氢化,所得烷烃的系统名称是_____。
的系统名称是_____,将其在催化剂存在 下完全氢化,所得烷烃的系统名称是_____。
(3)苯的同系物中,有的侧链能被酸性高锰酸钾溶液氧化,生成芳香酸,反应如下:
 (R、R′表示烷基或氢原子)
(R、R′表示烷基或氢原子)
①现有苯的同系物甲和乙,分子式都是C10H14。甲不能被酸性高锰酸钾溶液氧化为芳香 酸,它的结构简式是_____;乙能被酸性高锰酸钾溶液氧化为分子式为C8H6O4的芳香
酸,则乙可能的结构有______种。
②有机物丙也是苯的同系物,分子式也是C10H14,它的苯环上的一溴代物只有一种。丙的 结构简式共有四种,写出其余三种:
 __________、_________________、_______________
__________、_________________、_______________
(4)已知:RCH=CHR![]() RCOOH+RCOOH。写出
RCOOH+RCOOH。写出![]() 在强氧化剂(足量酸性高锰酸钾溶液)条件下生成
在强氧化剂(足量酸性高锰酸钾溶液)条件下生成![]() 和另一种理论最终产物_____(写出其结构式)。
和另一种理论最终产物_____(写出其结构式)。
(5)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流 程:![]()
①_____(填反应类型)②_____(填该物质的电子式)③______(填反应类 型)写出第一步的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物a(![]() )、b(
)、b( )、c(
)、c( )的说法正确的是
)的说法正确的是
A. b、c互为同系物 B. a、b互为同分异构体
C. c分子的所有原子不可能在同一平面上 D. a、b、c均能与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式______________________________。
(2)利用烟道气中的SO2生产Na2S2O5的工艺为:

①pH=4.1时,Ⅰ中为__________溶液(写化学式)。
②工艺中加入Na2CO3固体、并再次充入SO2的目的是__________。
(3)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.01000 mol·L-1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为_____________,该样品中Na2S2O5的残留量为____________g·L-1(以SO2计)。
II、高铁酸钾是一种新型、高效、多功能水处理剂。某学习小组设计如下方案制备高铁酸钾:
![]()
(1)①高铁酸钾中铁元素的化合价为________。
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,冰水浴中反应1 h。发生的离子反应如下:(____)Fe3++ ( ) ClO-+ ( )[ ]==( ) FeO42-+( )Cl-+( ) H2O,完成并配平上述反应的化学方程式。
(2) 高铁酸钾和水发生反应,生成物能吸附杂质净水,同时还产生气体,写出反应的离子方程式:_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com