
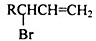
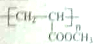 ,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
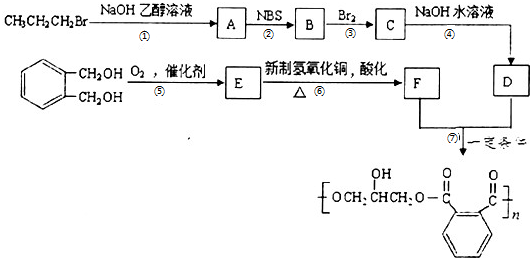
,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH. 分析 CH3CH2CH2Br在NaOH的乙醇溶液中加热发生消去反应生成丙烯CH3CH=CH2,A为丙烯CH3CH=CH2,结合信息,丙烯在NBS作用下发生取代反应生成的B为3-溴丙烯,3-溴丙烯与溴发生加成反应生成的C为1,2,3-三溴丙烷,C在NaOH的水溶液中水解生成的D为丙三醇CH2OHCHOHCH2OH,临二苯甲醇被氧化生成的E为邻二苯甲醛,E与新制氢氧化铜反应酸化后生成的F为临二苯甲酸,临二苯甲酸与丙三醇在一定条件下反应生成醇酸树脂,据此分析.
解答 解:(1)A为丙烯CH3CH=CH2,结合信息,丙烯在NBS作用下生成的B为3-溴丙烯,含有的官能团有溴原子和碳碳双键,故答案为:溴原子和碳碳双键;
(2)丙烯在NBS作用下发生取代反应生成的B为3-溴丙烯,临二苯甲醇被氧化生成的E为邻二苯甲醛,故答案为:取代反应;氧化反应;
(3)CH3CH2CH2Br在NaOH的乙醇溶液中加热发生消去反应生成丙烯CH3CH=CH2,故答案为:NaOH的乙醇溶液;
(4)a、临二苯甲醇被氧化生成的E为邻二苯甲醛,1molE与银氨溶液反应生成4molAg,故a错误;
b、E与新制氢氧化铜反应酸化后生成的F为临二苯甲酸,1mol F能与NaHCO3反应产生2mol CO2,故b正确;
c、检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、过量硝酸酸化、硝酸银溶液,故c错误;
d、临二苯甲醇被氧化生成的E为邻二苯甲醛,其催化剂可能是Cu或Ag,故d正确;
故答案为:bd;
(5)C为1,2,3-三溴丙烷,C在NaOH的水溶液中水解生成的D为丙三醇CH2OHCHOHCH2OH,化学方程式为CH2BrCHBrCH2Br+3NaOH$→_{△}^{水}$CH2OHCHOHCH2OH+3NaBr,
故答案为:CH2BrCHBrCH2Br+3NaOH$→_{△}^{水}$CH2OHCHOHCH2OH+3NaBr;
(6)B为3-溴丙烯,其在NaOH的水溶液中水解生成CH2=CHCH2OH,丙烯醇氧化生成丙烯醛,丙烯醛氧化生成丙烯酸,丙烯酸与甲醇发生酯化反应生成丙烯酸甲酯,丙烯酸甲酯通过加聚反应生成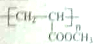 ,合成路线为:CH2=CHCH2Br$→_{△}^{NaOH水溶液}$CH2=CHCH2OH$→_{△}^{Cu}$CH2=CHCHO$→_{△}^{新制氢氧化铜}$CH2=CHC0OH$→_{△}^{甲醇、浓硫酸}$CH2=CHCOOCH3$\stackrel{引发剂}{→}$
,合成路线为:CH2=CHCH2Br$→_{△}^{NaOH水溶液}$CH2=CHCH2OH$→_{△}^{Cu}$CH2=CHCHO$→_{△}^{新制氢氧化铜}$CH2=CHC0OH$→_{△}^{甲醇、浓硫酸}$CH2=CHCOOCH3$\stackrel{引发剂}{→}$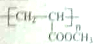 ,
,
故答案为:CH2=CHCH2Br$→_{△}^{NaOH水溶液}$CH2=CHCH2OH$→_{△}^{Cu}$CH2=CHCHO$→_{△}^{新制氢氧化铜}$CH2=CHC0OH$→_{△}^{甲醇、浓硫酸}$CH2=CHCOOCH3$\stackrel{引发剂}{→}$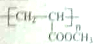 .
.
点评 本题考查了有机物的合成,难度不大,明确物质具有的官能团确定其具有的性质,注意官能团的变化,答题时要注意基础知识的灵活运用.


科目:高中化学 来源: 题型:选择题
| A. | 酯化反应的反应物之一肯定是醇 | B. | 酯化反应一般不需要加热 | ||
| C. | 酯化反应是有限度的 | D. | 酯化反应一般需要催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鱼虾放久了会产生不愉快的腥臭气味,应当用水冲洗,并在烹调时加入少量食醋 | |
| B. | 聚乙烯塑料制品是非环境友好材料,不应制造和使用这类合成材料 | |
| C. | 被蜂蚁蜇咬会感到疼痛难忍,这是蜂蚁咬人时将甲酸注入人体的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 医用酒精可用于皮肤消毒,其原因在于可以使蛋白质发生变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测得该消毒液的pH约为12 | |
| B. | 该消毒液中,Fe3+、K+、NO${\;}_{3}^{-}$、CH3CHO可以大量共存 | |
| C. | 向该消毒液中滴入少量Na2SO3溶液,反应的离子方程为:SO${\;}_{3}^{2-}$+ClO-=Cl-+SO${\;}_{4}^{2-}$ | |
| D. | 向该消毒液中加入浓盐酸,每产生1mol Cl2,转移电子数约为2×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. ,
,查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com