
某实验小组的同学在获得了如下资料的情况下,利用下面的装置来探究二氧化氮与碳酸氢钠溶液反应的产物及反应的机理。
资料:①亚硝酸是一种弱酸,酸性较碳酸酸性强;
②亚硝酸不稳定,很易分解:3HNO2===HNO3+2NO↑+H2O。
实验步骤如下:
①检查装置气密性;
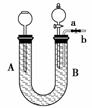
②在U形管中盛满蒸馏水,从b处通入二氧化氮气体,在U形管的B处得到无色气体,打开分液漏斗活塞,使少量气体进入分液漏斗,在分液漏斗中看到有红棕色气体;
③在U形管中盛满饱和碳酸氢钠溶液,从b处通入二氧化氮气体,在U形管的B处也得到无色气体,打开分液漏斗活塞,使少量气体进入分液漏斗,在分液漏斗中却看不到红棕色气体;
④将③中B处无色气体通过导管b通入足量澄清石灰水中有白色沉淀生成;
⑤将U形管中盛满氢氧化钠溶液,从b处通入二氧化氮时在B处得不到任何气体。
请回答下列各题:
(1)检查装置气密性的方法为__________________________________________________。
(2)在②中B处得到的无色气体是__________;用两个化学方程式表示二氧化氮与水反应的化学反应机理:_________________________________________________________________。
(3)在③中B处得到的无色气体(单一纯净)是________;只得到该无色气体的原因是________________________________________________________________________。
(4)取出③中得到的溶液,加入足量稀盐酸,预测可观察到的现象________________________________________________________________________。
(5)写出⑤中发生反应的化学方程式__________________________________________。
答案 (1)关闭分液漏斗的活塞,夹紧止水夹b,从长颈漏斗加水,长颈漏斗中形成一段稳定的水柱,证明气密性良好
(2)NO 2NO2+H2O===HNO2+HNO3、3HNO2===HNO3+2NO↑+H2O
(3)CO2 NO2与水反应生成HNO2和HNO3,二者的酸性都比碳酸的酸性强,因而与NaHCO3反应生成CO2
(4)产生无色气体,在空气中变为红棕色
(5)2NO2+2NaOH===NaNO3+NaNO2+H2O
解析 解答该题的关键是能及时迁移应用资料卡中的信息,结合已掌握的氮及其化合物的性质,合理解释每步实验现象。①带有长颈漏斗的装置检查气密性,一般都采用“液差法”,首先应注意密封一端;②说明NO2与水反应生成NO,印证3NO2+H2O===2HNO3+NO的存在;③、④说明NO2与NaHCO3溶液反应,气体产物只有CO2,没有NO,从而否定NO2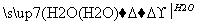
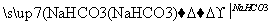 CO2的常规认识,再根据资料卡中的信息,预测可能是NO2与水反应生成HNO3和HNO2,生成的HNO2立即与NaHCO3反应生成了稳定的NaNO2,不能分解产生NO。⑤更进一步验证了上述推测的正确性。
CO2的常规认识,再根据资料卡中的信息,预测可能是NO2与水反应生成HNO3和HNO2,生成的HNO2立即与NaHCO3反应生成了稳定的NaNO2,不能分解产生NO。⑤更进一步验证了上述推测的正确性。


科目:高中化学 来源: 题型:
25 ℃时,将1 mol/L的醋酸钠溶液用水稀释至0.1 mol/L,溶液中增大的是( )
A.c(OH-) B.c(CH3COOH) C. 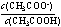 D. c(H+)
D. c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
硫化氢(H2S)是一种无色剧毒有臭鸡蛋气味的气体,蛋白质腐败和某些生命活动中均可以产生硫化氢,在工农业生产及科研活动中有重要的用途。
资料:①H2S可溶于水,其水溶液叫氢硫酸,是一种二元弱酸。
②FeS是一种不溶于水的黑褐色块状固体,能溶于盐酸或稀硫酸生成H2S。
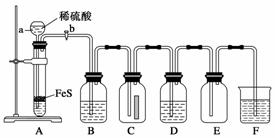
(1)某化学实验小组设计了制取少量H2S并验证其性质的实验,如下图所示。B中盛放CuSO4溶液,C中放有湿润的蓝色石蕊试纸,D中盛放FeCl3溶液。
请回答下列问题:
①装置A中仪器a的名称是__________。写出装置A中发生反应的离子方程式____________;
②B中有黑色沉淀产生,B中发生反应的化学方程式为____________。工业上利用该反应检验Cu2+的存在,并使用H2S作为除去废水中某些重金属离子的沉淀剂;
③D中只有浅黄色沉淀产生,且溶液变浅绿色。写出发生反应的离子方程式______________。检验溶液中的Fe3+已经反应完全的操作过程______________。
(2)下图是实验室制取气体的常用反应装置。

现在该小组在实验室中要用硫化亚铁和稀硫酸制备较大量的H2S气体,可选择装置________。有同学选择了乙,请指出采用乙装置制取硫化氢气体的主要缺点________________。
(3)为进一步探究-2价硫的化合物与+4价硫的化合物发生反应的条件,该小组同学又设计了下列实验。
| 实验操作 | 实验现象 | |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2∶1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
①根据上述实验,可以得出结论:在________条件下,+4价硫的化合物可以氧化-2价硫的化合物。
②已知:电离平衡常数:H2S Ka1=1.3×10-7;Ka2=7.1×10-15
H2SO3 Ka1=1.7×10-2;Ka2=5.6×10-8
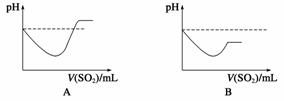
将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是________(填序号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下列方法测定某水样中O2的含量。
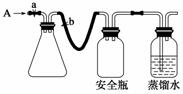
(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为____________________。
再用I-将生成的MnO(OH)2还原为Mn2+,反应的离子方程式为MnO(OH)2+2I-+4H+===Mn2++I2+3H2O。然后用Na2S2O3标准溶液滴定生成的I2,反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是________;
②用注射器抽取某水样20.00 mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸溶液;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入2~3滴________作指示剂;
⑧用0.005 mol·L-1 Na2S2O3滴定至终点。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________(单位:mg·L-1)。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将________(填“偏大”、“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2====2X+2H2O,下列说法中正确的是( )
A.X的化学式为AgS
B.银针验毒时,空气中氧气失去电子
C.反应中Ag和H2S均是还原剂
D.每生成1 mol X,反应转移2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种短周期元素,它们的结构、性质等信息如下表所述:
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 可用作制冷剂,元素的气态氢化物极易溶于水 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式 。
(2)B元素在周期表中的位置 ;离子半径:B A(填“大于”或“小于”)。
(3)C原子的电子排布图是 ,其原子核外有 个未成对电子,能量最高的电子为 轨道上的电子,其轨道呈 形。
(4)D原子的电子排布式为 ,D-的结构示意图是 。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为 。与D的氢化物的水化物反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
向10 mL 0.1 mol·L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液xmL,下列叙述正确的是( )
A.x=10时,溶液中有N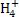 、Al
、Al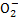 、S
、S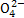 ,且c(N
,且c(N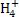 )>c(S
)>c(S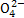 )
)
B.x=10时,溶液中有N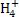 、Al3+、S
、Al3+、S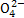 ,且c(N
,且c(N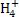 )>c(Al3+)
)>c(Al3+)
C.x=30时,溶液中有Ba2+、Al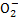 、OH-,且c(OH-)<c(Al
、OH-,且c(OH-)<c(Al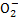 )
)
D.x=30时,溶液中有Ba2+、Al3+、Al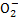 ,且c(OH-)=c(Ba2+)
,且c(OH-)=c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列装置不能达到有关实验目的的是( )
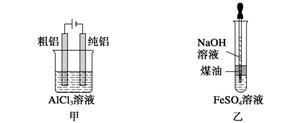
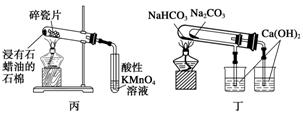
A.用甲图装置电解精炼铝
B.用乙图装置制备Fe(OH)2
C.丙图装置酸性KMnO4溶液中出现气泡且颜色逐渐褪去
D.用丁图装置验证NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com