
分析 氯化铁为强酸弱碱盐水解显酸性,将Na2S溶液滴加到FeCl3溶液中,有单质硫生成,反应方程式为:2Fe3++S2-═2Fe2++S↓,依据氧化性强弱规律解答;
硫化钠溶液为强碱弱酸盐水解显碱性,将FeC13溶液滴加到Na2S溶液中生成的是Fe2S3,离子方程式为:Fe3++S2-=Fe2S3,依据溶度积规则解答;
解答 解:氯化铁为强酸弱碱盐水解显酸性,将Na2S溶液滴加到FeCl3溶液中,有单质硫生成,反应方程式为:2Fe3++S2-═2Fe2++S↓,反应中三价铁离子为氧化剂,硫为氧化产物,氧化剂的氧化性大于氧化产物的氧化性,所以
酸性条件氧化性:Fe3+>S;
硫化钠溶液为强碱弱酸盐水解显碱性,将FeC13溶液滴加到Na2S溶液中生成的是Fe2S3,离子方程式为:Fe3++S2-=Fe2S3,说明硫化铁溶解度小于氢氧化铁,给出Fe3+能力:Fe(OH)3>Fe2S3;
故答案为:酸性条件氧化性:Fe3+>S;给出Fe3+能力:Fe(OH)3>Fe2S3;
点评 本题考查了氧化还原反应规律、溶度积规则,明确相关知识是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| H2CO3 | Ka1=4.3×10-7 | HClO | Ka=2.95×10-8 |
| Ka2=5.61×10-11 | AgCl | Ksp=1.77×10-10 | |
| CH3COOH | Ka=1.76×10-5 | Ag2CrO4 | Ksp=1.12×10-12 |
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| FeCl3溶液体积/mL | 100 | 100 | 100 | 100 |
| 加入粉末质量/g | 3 | 6.6 | 9 | 12 |
| 剩余粉末质量/g | 0 | 0.64 | 3.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青铜、碳素钢和石英都是合金 | |
| B. | 陶瓷、玻璃和水泥都是无机非金属材料 | |
| C. | 乙醇与乙醛互为同分异构体,都能发生银镜反应 | |
| D. | 油脂皂化和蛋白质水解都是由高分子生成小分子的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率可用某时刻生成物的物质的量来表示 | |
| B. | 在同一反应中,用反应物或生成物表示的化学反应速率的值是相对的 | |
| C. | 化学反应速率是指反应进行的时间内,反应物浓度的减少或生成物浓度的增加 | |
| D. | 可用单位时间内氢离子物质的量浓度的变化来表示氢氧化钠和硫酸的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
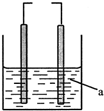 如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )| A. | ① | B. | ② | C. | ①② | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧原子能量最高的电子的电子云图: | |
| B. | 35Cl与37Cl互为同素异形体 | |
| C. | CH4分子的比例模型: | |
| D. | 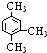 的命名:1,3,4-三甲苯 的命名:1,3,4-三甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | OH-+CO2→HCO3- | |
| B. | 2OH-+CO2→CO32-+H2O | |
| C. | Ca2++2OH-+CO2→CaCO3↓+H2O | |
| D. | Ca2++4OH-+2CO2→CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
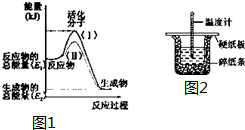 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图1,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图1,然后回答问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com