
【题目】下图是几种有机物的转换关系,请按要求填空:

已知:A是来自石油的重要有机化工原料,对水果有催熟作用;75%的B可用于医用消毒;E是 具有果香味的有机物,结构简式为C4H8O2;F是一种高聚物,可制成多种包装材料。
(1)G的名称是_____________; F的链节是_____
(2)反应类型:①__________; ③_____
(3)书写反应方程式: ②_____
(4)下列关于 A 和 F 的叙述正确的是_____
A.A 常温下是气体,为纯净物;F 常温下是固体,为混合物
B.A 和 F 都能使酸性高锰酸钾溶液褪色
C.取等质量的 A 和 F 完全燃烧后,生成的 CO2 和 H2O 的质量分别相等
D.取等物质的量的 A 和 F 完全燃烧后,生成的 CO2 和 H2O 的物质的量分别相等
(5)与 E 互为同分异构体,且含有“—COO—”结构的有机物还有____________种。
【答案】 1,2—二溴乙烷 —CH2—CH2— 加成反应 酯化反应 2 CH3CH2OH+ O2 ![]() 2 CH3CHO + 2H2O A、C 5
2 CH3CHO + 2H2O A、C 5
【解析】A是来自石油的重要有机化工原料,对水果有催熟作用,则A为CH2=CH2;75%的B可用于医用消毒,B为乙醇,A和水发生加成反应生成B为CH3CH2OH;B被催化氧化生成C为CH3CHO,A和溴发生加成反应生成G为CH2BrCH2Br;F是一种高聚物,可制成多种包装材料,则F为![]() ;E是具有果香味的有机物,B为酸性高锰酸钾溶液氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3。
;E是具有果香味的有机物,B为酸性高锰酸钾溶液氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3。
(1)G为CH2BrCH2Br,G的名称是 1,2-二溴乙烷,F为聚乙烯,链节是-CH2-CH2-,故答案为: 1,2-二溴乙烷;-CH2-CH2-;
(2)根据分析,反应①为乙烯与水的加成反应;反应③为乙醇和乙酸的酯化反应,故答案为:加成反应; 酯化反应;
(3)反应②为乙醇的催化氧化,反应的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO + 2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO + 2H2O,故答案为:2CH3CH2OH+O2![]() 2CH3CHO + 2H2O;
2CH3CHO + 2H2O;
(4)A为乙烯,F为聚乙烯。A.乙烯常温下为气体,属于纯净物,聚乙烯,常温下是固体,聚合度不同,属于混合物,故A正确;B.聚乙烯没有碳碳双键,不能使酸性高锰酸钾溶液褪色,故B错误;C.乙烯与聚乙烯的最简式相同,等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等,故C正确;D.乙烯与聚乙烯分子中含有碳原子数目不同、氢原子数目不同,取等物质的量的乙烯和聚乙烯完全燃烧后,生成的CO2的物质的量不相等,生成H2O的物质的量也不相等,故D错误,故选AC;
(5)E为CH3COOCH2CH3,与E互为同分异构体,且含有“—COO—”结构的有机物还有HCOOCH2CH2CH3,HCOOCH2(CH3)2,CH3CH2COOCH3,CH3CH2CH2COOH,(CH3)2CHCOOH,共5种,故答案为:5。


科目:高中化学 来源: 题型:
【题目】(1)已知2 mol氢气燃烧生成液态水时放出572 kJ的热量,反应方程式是2H2(g)+O2(g)===2H2O(l)。请回答下列问题:
(1)①该反应的生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572 kJ。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g) ![]() 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l) ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式是_________________ 。
(3)已知下列反应的热化学方程式:
①6C(s)+5H2(g)+3N2(g)+9O2(g)===2C3H5(ONO2)3(l) ΔH1
②2H2(g)+O2(g)===2H2O(g) ΔH2
③C(s)+O2(g)===CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)===12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36 号元素),对 比中学常见元素周期表思考扇形元素周期表的 填充规律,并用化学用语.回答下列问题:
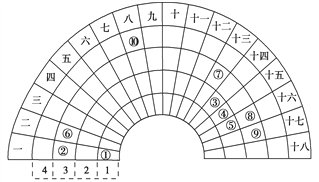
(1)若①~⑩分别代表十种元素,则⑧代表的元素在常见周期表中的位置是____________
(2)比较元素最高价氧化物对应水化物的碱性:②_____________⑥(填“>”或“<”)
(3)写出一种由①、④、⑤三种元素形成的常见离子化合物:___________,设计一个简单的实验检验其阳离子的存在:___________________。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________。
(5)①、③、⑤三种元素形成的18 电子结构的化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②的最高价氧化物对应的水化物作电解质的燃料电池的负极反应式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不正确的是( )
A.在熔化和溶解时均不导电的化合物,叫做非电解质
B.电解质,非电解质都对化合物而言,单质不在此范畴
C.在水中的电解质一定都导电
D.水是极弱的电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下将CO2气体缓缓地通入到含2 mol KOH、1 mol Ba(OH)2和2 mol KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是

A.A~B段和C~D段发生的反应相同
B.B~C段反应的离子方程式是A1O2-+2H2O+CO2=Al(OH)3↓+HCO3-
C.V=134.4 L,n=3mol
D.D点所得溶液中离子浓度的关系为:c(K+)>c(CO32-)>c(OH﹣)>c(HCO3-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中![]() 的含量变化来监测核电站是否发生放射性物质泄漏。下列有关
的含量变化来监测核电站是否发生放射性物质泄漏。下列有关![]() 的叙述中错误的是
的叙述中错误的是
A. ![]() 的化学性质与
的化学性质与![]() 相同 B.
相同 B. ![]() 的原子序数为53
的原子序数为53
C. ![]() 的原子核外电子数为78 D.
的原子核外电子数为78 D. ![]() 的原子核内中子数多于质子数
的原子核内中子数多于质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在稀溶液中,强酸跟强碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:

(1)该图中有两处未画出,它们是______________、________________。
(2)做一次完整的中和热测定实验,温度计需使用________次。
(3)把温度为15.0 ℃,浓度为0.5 mol·L-1的酸溶液和0.55 mol·L-1的碱溶液各50 mL混合(溶液密度均为1 g·mL-1),生成溶液的比热容c=4.18 J · g-1 · ℃-1,轻轻搅动,测得酸碱混合液的温度变化数据如下:
反应物 | 起始温度t1/℃ | 终止温度t2/℃ | 中和热 |
HCl+NaOH | 15.0 | 18.4 | ΔH1 |
HCl+NH3·H2O | 15.0 | 18.1 | ΔH2 |
①计算上述第一组实验测出的中和热ΔH1=______。
②写出HCl+NH3·H2O的热化学方程式:____________________________________。
③两组实验结果差异的原因是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )

A.反应①②③④⑤均属于氧化还原反应和离子反应
B.反应⑤说明该条件下铝的还原性强于锰
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com