
| A. | 加热可增强纯碱溶液去污能力:CO32-+2H2O?H2CO3+2OH- | |
| B. | 用醋酸溶液除水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO2+2CaSO4 | |
| D. | 碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀:CO32-+Ca2+=CaCO3↓ |
分析 A.碳酸根离子的水解分步进行,离子方程式写出第一步的水解即可;
B.醋酸为弱电解质,离子方程式是中醋酸不能拆开,需要保留分子式;
C.生石灰为碳酸钙,碳酸钙与氧气、二氧化硫在加热条件下能够反应生成硫酸钙和二氧化碳气体;
D.碳酸氢钠电离出碳酸氢根离子和钠离子,碳酸氢根离子不能拆开;氢氧化钙少量,离子方程式按照氢氧化钙的化学式组成书写.
解答 解:A.盐的水解为吸热反应,则加热可增强纯碱溶液去污能力,正确的离子方程式为:CO32-+H2O?HCO3-+OH-,故A错误;
B.碳酸钙和醋酸在离子方程式中都不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.向煤中加入石灰石可减少煤燃烧时SO2的排放,反应的化学方程式为:2CaCO3+O2+2SO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO2+2CaSO4,故C正确;
D.溶液与少量澄清石灰水混合出现白色沉淀,离子方程式按照氢氧化钙的化学式书写,正确的离子方程式为Ca2++2HCO3-+2OH-=CO32-+CaCO3↓+2H2O,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 用白醋除铁锈:Fe2O3+6H+═3H2O+2Fe3+ | |
| B. | 向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+BaCO3↓ | |
| C. | AlCl3溶液中滴加浓氨水至过量:Al3++4NH3˙H2O═AlO2-+4NH4++2H2O | |
| D. | MnO2与浓盐酸反应制取Cl2:MnO2+4H++4Cl-═Mn2++2Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g甲烷含有的电子数为NA | |
| B. | 1 L0.1 mol/L NaHCO3溶液中含有的HCO3- 数目为0.1 NA | |
| C. | 1 L PH=1的硫酸溶液中含有的H+ 数为0.2 NA | |
| D. | 标准状况下,2.24 LCO和CO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 9种 | C. | 12种 | D. | 15种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 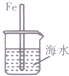 图中,插人海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. | 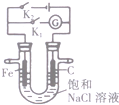 图中,闭合K2,铁电极的腐蚀速率比闭合K1时慢 | |
| C. | 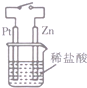 图中,接通开关时,Zn的腐蚀速率增大,Zn上放出气体的速率也增大 | |
| D. | 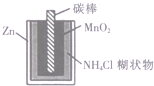 图中,锌锰电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
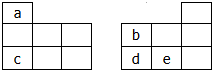 如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.| A. | 原子半径:b>c | |
| B. | 由a、b、e三种元素形成的化合物可能是离子化合物 | |
| C. | c与e以原子个数比2:1形成的化合物能促进水的电离 | |
| D. | 氢化物的稳定性:b<d. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
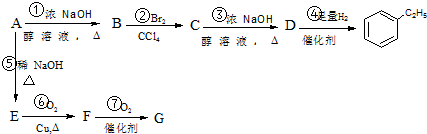
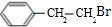 ; B
; B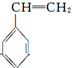 ; D
; D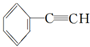 ;G
;G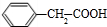 .
.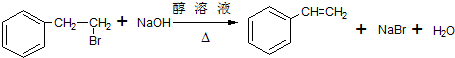 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
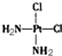 具有抗癌作用,而
具有抗癌作用,而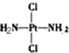 没有抗癌作用,对此下列叙述正确的是( )
没有抗癌作用,对此下列叙述正确的是( )| A. | 两者为同一物质,都是以Pt原子为中心的四面体结构 | |
| B. | 两者为同一物质,都是以Pt原子为中心的平面结构 | |
| C. | 两者互为同分异构体,都是以Pt原子为中心的四面体结构 | |
| D. | 两者互为同分异构体,都是以Pt原子为中心的平面结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com