
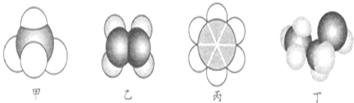
| A. | 22.4 L甲中含有10 mol电子 | |
| B. | 乙与乙的加聚产物都能使溴水褪色 | |
| C. | 丙不能与溴水、酸性高锰酸钾溶液发生反应 | |
| D. | 丙、丁都可以萃取溴水中的溴单质 |
分析 由图可知,甲为甲烷,乙为乙烯,丙为苯,丁为乙醇.
A.气体存在的条件未知,不能确定物质的量;
B.乙烯中含双键,可发生加成、加聚反应,但加聚产物不含碳碳双键;
C.苯性质稳定,与溴水、高锰酸钾不反应;
D.乙醇与水混溶.
解答 解:由图可知,甲为甲烷,乙为乙烯,丙为苯,丁为乙醇.
A.气体存在的条件未知,则不能确定22.4 L甲烷的物质的量,不能确定电子数,故A错误;
B.乙烯的加聚产物为聚乙烯,不含碳碳双键,不能使溴水褪色,故B错误;
C.苯性质稳定,不含碳碳双键,与溴水、高锰酸钾不反应,故C正确;
D.乙醇与水混溶,不能用于萃取剂,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握比例模型及对应化合物的性质为解答的关键,侧重常见几种烃和乙醇性质及结构的考查,题目难度不大.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:选择题
| A. | (A-x+m)mol | B. | (A-x-m)mol | C. | $\frac{W}{A}$(A-x+m)mol | D. | $\frac{W}{A}$(A-x-m)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

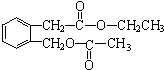 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$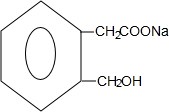 +CH3COONa+CH3CH2OH+H2O;反应类型是水解反应(或取代反应);
+CH3COONa+CH3CH2OH+H2O;反应类型是水解反应(或取代反应);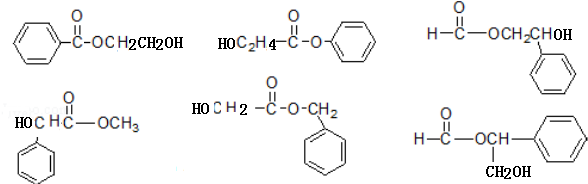 (任写两个).
(任写两个).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 步骤①所用仪器包括蒸发皿、酒精灯、玻璃棒等 | |
| B. | 步骤②所用的浓硝酸应保存在带橡皮塞的棕色试剂瓶中 | |
| C. | 步骤③可以不做,改为将悬浊液静置一段时间 | |
| D. | 步骤④观察到溶液变红色,证明茶叶中含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Y在空气中燃烧一定生成Y2O2 | B. | Z只能形成两种含氧酸根 | ||
| C. | X-半径一定比Y+半径大 | D. | W 的氢化物一定比Z的氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
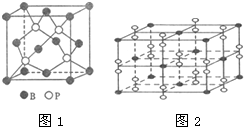 As、N、0等非金属元素的化合物在工业生产中有重要的应用.
As、N、0等非金属元素的化合物在工业生产中有重要的应用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
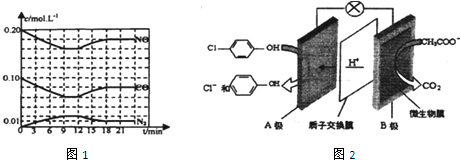
 )的酸性废水,可利用微生物电池法除去,其原理如图2所示
)的酸性废水,可利用微生物电池法除去,其原理如图2所示查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 地沟油经过处理,可用来制造肥皂 | |
| C. | 漂白粉长期暴露在空气中会变质失效 | |
| D. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (不包括A)
(不包括A) ;反应类型是酯化反应(或取代反应).
;反应类型是酯化反应(或取代反应). .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com