
| A. | 8+$\frac{1}{2}$ lg2 | B. | 9+lg2 | C. | 10+$\frac{1}{2}$ lg2 | D. | 11+2lg2 |
分析 Mn2+沉淀较为完全时,c(Mn2+)≤1×10-5mol/L,根据Ksp求出OH-离子的浓度,再根据Kw求出氢离子的浓度,然后计算出pH,据此进行计算.
解答 解:Mn2+沉淀较为完全时的浓度≤1×10-5mol/L,已知Ksp=c(Mn2+)×c2(OH-),
则c(OH-)≥$\sqrt{\frac{{K}_{sp}}{c(M{n}^{2+})}}$=$\sqrt{\frac{2×1{0}^{-13}}{1×1{0}^{-5}}}$mol/L=$\sqrt{2}$×10-4mol/L,
则c(H+)≤$\frac{{K}_{W}}{c(O{H}^{-})}$=$\frac{1×1{0}^{-14}}{\sqrt{2}×1{0}^{-4}}$mol/L=$\frac{\sqrt{2}}{2}$×10-10mol/L,
所以pH≥-lg$\frac{\sqrt{2}}{2}$×10-10=10+$\frac{1}{2}$lg2,
故选C.
点评 本题考查溶度积常数及溶液pH的计算,题目难度中等,注意掌握难溶物溶度积常数的概念及计算方法,明确Mn2+沉淀较为完全时c(Mn2+)≤1×10-5mol/L为解答关键.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E五种元素是周期表中前四周期的元素.只有A、B、C为金属且同周期,原子序数A<B<C.A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道.D原子最外层电子数是其周期序数的三倍.E能与D形成化合物ED2,可用于自来水的消毒.
A、B、C、D、E五种元素是周期表中前四周期的元素.只有A、B、C为金属且同周期,原子序数A<B<C.A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道.D原子最外层电子数是其周期序数的三倍.E能与D形成化合物ED2,可用于自来水的消毒.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=Z+A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用新制氢氧化铜悬浊液能鉴别葡萄糖、甘油、乙醛、乙酸 | |
| B. | 用酸性高锰酸钾即可检验CH2=CHCHO中的碳碳双键 | |
| C. | 为检验氯乙烷中的氯元素,在水解液中滴加稀硫酸酸化,再滴入AgNO3溶液,产生白色沉淀 | |
| D. | 用溴水即可鉴别溴苯、苯、己烯与苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn(l)=Zn(g)△H=$\frac{1}{2}$(△H1-△H2 ) | |
| B. | 用硅制作的太阳能电池是将化学能转化为电能 | |
| C. | 增加Zn(g)的量,△H2变大 | |
| D. | 以Zn片、铜片和稀硫酸构成的原电池,Zn片表面有气泡产生. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
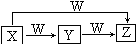 X、Y、Z、W均为中学化学常见物质,一定条件下它们有如图所示的转化关系(某些产物已略去),下列说法错误的是( )
X、Y、Z、W均为中学化学常见物质,一定条件下它们有如图所示的转化关系(某些产物已略去),下列说法错误的是( )| A. | 若X为HNO3,则W可能为Fe | |
| B. | 若W为O2,X可能是S | |
| C. | 若W为O2,则Z可能为NO | |
| D. | X→Z的离子反应可能为Al3++4OH-=AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C、D、E、F是周期表中前四周期的六种元素,它们的性质或结构信息如表,请根据信息回答下列问题:
已知A、B、C、D、E、F是周期表中前四周期的六种元素,它们的性质或结构信息如表,请根据信息回答下列问题:| 元素 | 性质或结构信息 |
| A | 单质为黄色粉末,难溶于水,能形成2种二元含氧酸 |
| B | M层有1个未成对的p电子,核外电子总数大于7 |
| C | 与锂形成的合金常用于航天飞行器,单质能溶于强酸和强碱 |
| D | S电子总数比p电子总数少2个,单质或氧化物均具有很高的熔、沸点 |
| E | 周期表中电负性最大的元素 |
| F | 最外层有2个电子,但次外层有18个电子 |
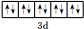 .
.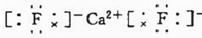 .已知该化合物晶胞$\frac{1}{8}$的体积为2.0×10-23cm3,该离子化合物的密度为3.2g/cm3(保留一位小数).
.已知该化合物晶胞$\frac{1}{8}$的体积为2.0×10-23cm3,该离子化合物的密度为3.2g/cm3(保留一位小数).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氢氟酸在玻璃上镌刻图案:4I++SiO2═H2O+Si4+ | |
| B. | 向Cu2+、Fe3+混合液中加入CuO除去Fe3+;3H2O+3CuO+2Fe3+═2Fe(OH)3+3Cu2+ | |
| C. | 亚硫酸氢钠溶液显酸性:HSO3-═H++SO32- | |
| D. | 用盐酸与碳酸钠反应证明氯的非金属性强与炭:2H++CO32-═CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com