
 ,故答案为:
,故答案为: ;
;

 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、氢化物的沸点为HnT<HnQ |
| B、L、R的单质与稀盐酸反应的速率为R>L |
| C、M与T形成的化合物具有两性 |
| D、L、Q形成的简单离子的核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
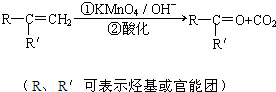
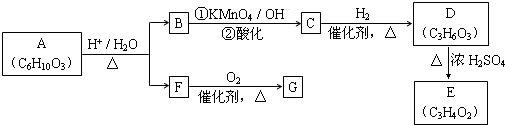
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、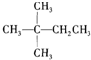 |
| B、CH3CH2CH2CH2CH3 |
C、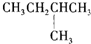 |
D、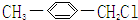 |
查看答案和解析>>
科目:高中化学 来源: 题型:
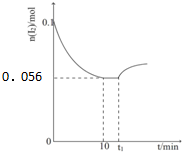 向1L密闭容器中加入I2和
向1L密闭容器中加入I2和 各0.1mol,在一定条件下,发生反应:I2(g)+
各0.1mol,在一定条件下,发生反应:I2(g)+ (g)?
(g)? (g)+2HI(g)△H>0 测得体系中n(I2)随时间t变化如图所示,下列有关说法错误的是( )
(g)+2HI(g)△H>0 测得体系中n(I2)随时间t变化如图所示,下列有关说法错误的是( )A、单位时间内生成等物质的量的 和 和 时,反应达到平衡 时,反应达到平衡 |
| B、0-10min内生成HI的反应速率0.0088mol.L-1.min-1 |
C、10min时, 的转化率为44.0% 的转化率为44.0% |
| D、t1后图线变化可能是反应体系温度升高所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组通过查阅资料得到如下信息,乙醇在加热条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如表所示.
某研究性学习小组通过查阅资料得到如下信息,乙醇在加热条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如表所示.| 溶解性(本身均可做溶剂) | 沸点(℃) | 密度(g/mL) | |
| 乙醇 | 与水混溶,易溶于有机溶剂 | 78.5 | 0.8 |
| 溴乙烷 | 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com