
对于以下反应:A(s)+3B(g)⇌2C(g)+D(g),在一定温度和容积固定的容器中,下列判断正确的是( )
|
| A. | 当容器内的压强不再变化,可以判断反应已经达到平衡 |
|
| B. | 往容器中通入稀有气体He,由于压强增大,所以反应速率增大 |
|
| C. | 往容器中加入少量A,反应速率增大 |
|
| D. | 若反应是放热反应,升高温度,正反应速率增大 |
考点:
化学平衡的影响因素.
专题:
化学平衡专题.
分析:
A、反应前后气体体积不变的化学反应,压强始终不变;
B、压强的增大,只有影响到反应物或生成物的浓度,才会影响化学反应速率;
C、A是固态,加入A不会影响化学反应速率;
D、无论反应放热还是吸热,升高温度正逆反应速率都会加快.
解答:
解:A、该反应,反应前后气体体积不变,所以体积不变时压强始终不变,故A错误;
B、恒容时通入He气,不会影响B、C、D的浓度和分压,反应速率不变,故B错误;
C、A是固态物质,加入少量A不会影响反应速率,故C错误;
D、无论反应放热还是吸热,升高温度正逆反应速率都会加快,故D正确;
故选D.
点评:
本题考查影响化学反应速率的因素,要熟记影响化学反应速率的主要因素有温度、浓度、压强、催化剂、接触面积等等,特别是压强的影响,要明确增大压强时,只有影响到反应物或生成物的浓度时才会影响反应速率.


科目:高中化学 来源: 题型:
已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,如图所示,则硼氮苯的四氯取代物(B3N3H2Cl4)的同分异构体的数目为( )

|
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:2NO2(g)2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为221的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的压强不再改变的状态 ⑦混合气体的平均摩尔质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦
C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示:

A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡到达B点。
(1)25℃时水的离子积为________________,100℃时水的离子积为________________。
(2)100℃时,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
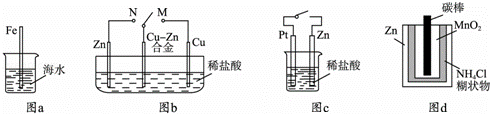
下列与金属腐蚀有关的说法正确的是( )
|
| A. | 图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
|
| B. | 图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小 |
|
| C. | 图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
|
| D. | 图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,将1mol CO和1mol水蒸气混合后发生如下变化:CO(g)+H2O(g)⇌CO2(g)+H2(g)若反应达平衡时测得CO转化率为25%,则平衡混合气体的密度为相同条件下H2密度的( )
|
| A. | 5.75倍 | B. | 11.5倍 | C. | 30.67倍 | D. | 46倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在一个恒温恒容的密闭容器中,可逆反应N2(g)+3H2(g)⇌2NH3(g)△H<0达到平衡的标志是 (填编号)
①反应速率v(N2):v(H2):v(NH3)=1:3:2
②各组分的物质的量浓度不再改变
③体系的压强不再发生变化
④混合气体的密度不变
⑤单位时间内生成n mol N2的同时,生成3n mol H2
⑥2V(N2正)=V(NH3逆)
⑦单位时间内3mol H﹣H键断裂的同时2mol N﹣H键也断裂
⑧混合气体的平均相对分子质量不再改变
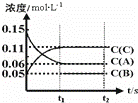
(2)向某体积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示.已知在反应过程中混合气体的平均分子量没有变化.请回答:
①密闭容器的体积是 L.
②若t1=15s时,则t0﹣t1阶段以C物质浓度变化表示的反应速率为v(C)= .
③写出反应的化学方程式: .
④B的起始物质的量是 .
(3)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式: .若1g水蒸气转化为液态水放热2.44kJ,则反应2H2(g)+O2(g)═2H2O(l)△H= kJ•mol﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是( )
|
| A. | 碳酸氢钙溶液与足量盐酸反应Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |
|
| B. | 稀盐酸和碳酸钙反应 CO32﹣+2H+=CO2↑+H2O |
|
| C. | 碳酸钠溶液与醋酸反应 CO32﹣+2H+=CO2↑+H2O |
|
| D. | 大理石溶于醋酸的反应 CaCO3+2CH3COOH=Ca2++2CH3COO﹣+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学平衡常数的说法中,正确的是( )
|
| A. | 在任何条件下,化学平衡常数都是一个定值 |
|
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 |
|
| C. | 化学平衡常数K只与温度、反应物浓度、体系的压强都有关 |
|
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com