
分析 求出水的物质的量n=$\frac{m}{M}$;然后根据水中含10个电子来分析;根据水中含2个H原子求出水中所含的氢原子的物质的量,从而求出含H原子个数相同的甲烷的物质的量,然后根据m=nM和V=nVm求出质量和体积,据此分析.
解答 解:水的物质的量n=$\frac{m}{M}$=$\frac{3.6g}{18g/mol}$=0.2mol,而水中含10个电子,故0.2mol水中含2mol电子即2NA个;而水中含2个H原子,故0.2mol水中含0.4mol氢原子,故含相同H原子个数的甲烷的物质的量为0.1mol,质量m=nM=0.1mol×16g/mol=1.6g,在标况下的体积V=nVm=0.1mol×22.4L/mol=2.24L.
故答案为:0.2;2NA;1.6g;2.24L.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:填空题

| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 |  | 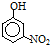 |  |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al原子的失电子能力逐渐减弱 | |
| B. | Si、P、S元素的最高正化合价依次降低 | |
| C. | C、N、O的原子半径依次减小 | |
| D. | Cl、Br、I的气态氢化物的稳态性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 和过量的 NaOH 溶液充分反应并加热,可生成标准状况下的 NH3 4.48L | |
| B. | 通入 H2S 气体,发生反应的离子方程式为:H2S+Fe2+=FeS↓+2H+ | |
| C. | Ca2+、ClO-、Cl-、Cu2+能在该溶液中大量共存 | |
| D. | Cl-、H+、I-、Na+不能在该溶液中大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
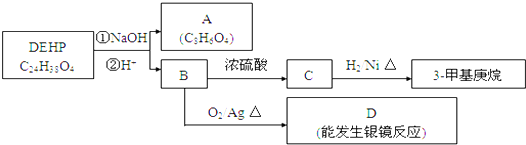
 +n HOCH2CH2OH
+n HOCH2CH2OH
 +(2n-1)H2O.
+(2n-1)H2O. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
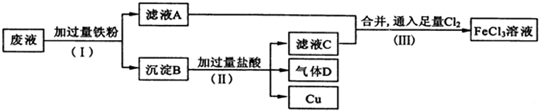
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com