
 .
. HSO3-+OH-;溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
HSO3-+OH-;溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).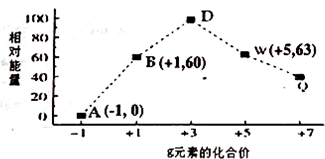
分析 x、y形成最简单的有机物M是重要的清洁能源,则M为CH4,可知x为H元素,y为C元素,金属元素e的单质在常温下能与水剧烈反应,应为Na,z元素原子的L层电子数为K层电子数的三倍,为O元素,z、f、g三种元素原子的最外层电子数之和为19,则f、g的原子的最外层电子数之和为13,应分别为S、Cl元素,以此解答该题.
解答 解:x、y形成最简单的有机物M是重要的清洁能源,则M为CH4,可知x为H元素,y为C元素,金属元素e的单质在常温下能与水剧烈反应,应为Na,z元素原子的L层电子数为K层电子数的三倍,为O元素,z、f、g三种元素原子的最外层电子数之和为19,则f、g的原子的最外层电子数之和为13,应分别为S、Cl元素,
(1)由以上分析可知g为Cl元素,位于周期表第三周期第 VIIA族,故答案为:第三周期第 VIIA族;
(2)yzf分子中所有原子的最外层都满足8电子结构,形成的化合物为CSO,具有二氧化碳的结构特点,电子式为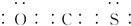 ,
,
故答案: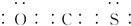 ;
;
(3)元素h与e处于同周期,且形成的简单离子是本周期中半径最小的,应为Al.Al单质与Fe2O3反应时,每消耗0.5molAl放热213kJ,则消耗2molAl放热852kJ,该反应的热化学方程式为2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-852kJ•mol-1,
故答案为:2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-852kJ•mol-1;
(4)仅由z、e、f三种元素形成的一种六核离子化合物为Na2SO3,为强碱若酸盐,溶于水后呈碱性,离子方程式为SO32-+H2O HSO3-+OH-,以第一步水解为主,溶液中离子浓度大小顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),
HSO3-+OH-,以第一步水解为主,溶液中离子浓度大小顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),
故答案为:SO32-+H2O HSO3-+OH-;c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);
HSO3-+OH-;c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);
(5)能量越低,离子越稳定,则最稳定的为Cl-,由化合价可知A为Cl-,B为ClO-,D为ClO2-,W为ClO3-,则D转化为A与W的离子方程式为3ClO2-=Cl-+2ClO3-,
故答案为:Cl-;3ClO2-=Cl-+2ClO3-.
点评 本题考查位置结构性质关系综合应用,为高考常见题型,推断元素是解题关键,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.


科目:高中化学 来源: 题型:选择题

| A. | 左边装置是氢氧燃料电池,右边装置是电镀池 | |
| B. | 电子流动方向:b→Zn→CuSO4(aq)→Cu→a | |
| C. | 一段时间后,左端溶液浓度变小,右端溶液浓度不变 | |
| D. | 左边装置中的电池反应为:2H2+O2=2H2O |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:选择题
下列叙述正确的是( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由其物质的量的多少决定
C.气体摩尔体积是指1mol任何气体所占的体积为22.4L
D.不同的气体,若体积不等,则它们所含的分子数一定不等
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
某合作学习小组讨论辨析下列说法,其中正确说法的数目为
①碱性氧化物都是金属氧化物,酸酐都是氧化物
②AlCl3溶液和Al(OH)3胶体的本质区别在于是否有丁达尔效应
③若规定0.024kg12C含有的原子数为阿伏加德罗常数,则标准状况下44gCO2的体积约为44.8L
④标准状况下,气体体积的大小取决于粒子数目和粒子间的平均距离
⑤同温同压下,等质量的二氧化硫气体和二氧化碳气体密度比为16:11,体积比为11:16
⑥把0.05mol氢氧化钡固体加入到100ml 1.0vmol/L盐酸中,溶液导电性基本不变
⑦活泼金属钾、钙、钠、镁、铝均由电解对应的熔融氧化物制得
⑧合金熔点、硬度都低于成分金属,青铜是使用最早的合金,钢是用量最大用途最广的合金
⑨同素异形体:C60、12C、金刚石、石墨
⑩工业合成氨是人工固氮的主要方法,工业生产玻璃、水泥、 冶炼铁都需要用到的原料是石灰石
冶炼铁都需要用到的原料是石灰石
A.3 B.5 C.4 D .7
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
CsICl2是一种碱金属的化合物,这类物质在化学反应中既可表现氧化性又可表现还原性,有关该物质的说法正确的是
A.Cs显+3价,I、Cl均显-1价
B.在CsICl2溶液中通入SO2气体,有硫酸生成
C.Cs显+1价,Cl显+1价,I显-3价
D.在CsICl2溶液中通入Cl2,有单质碘生成
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3-甲基-2-乙基戊烷 | |
| B. | (CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷 | |
| C. | 2-甲基-3-戊炔 | |
| D. | 邻甲基苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH(CH3)CH(CH3)OH:3-甲基-2-戊醇 | |
| B. | CH3CH(CH3)CH═CH2:3-甲基丁烯 | |
| C. | CH3CH2C(CH3)2CH3:2,2-甲基丁烷 | |
| D. | CH2Cl-CH2Cl:二氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 难氧化,易加成,难取代 | |
| B. | 能氧化,难加成,易取代 | |
| C. | 易氧化,易加成,难取代 | |
| D. | 因是单双键交替结构,故易加成为环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氢化物的沸点R>X | |
| B. | 原子半径:W>R>X | |
| C. | 气态氢化物的稳定性:X>Y | |
| D. | X、Z形成的化合物中可能含有共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com