
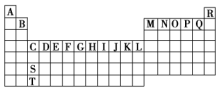
分析 (1)周期表中有7个主族,1、2、13、14、15、16、17列为主族;
(2)B在第2列,O在15列;ⅣB族为副族元素,在周期表中第4列;
(3)周期表中8、9、10三列为Ⅷ族;
(4)S所在的格内含15种元素;
(5)副族与Ⅷ统称为过渡元素;
(6)最外层8个电子的元素在0族.
解答 解:(1)周期表中有7个主族,1、2、13、14、15、16、17列为主族,由图可知,A、B、M、N、O、P、Q属于主族元素,
故答案为:A、B、M、N、O、P、Q;
(2)B、O分别属于ⅡA族、ⅤA族,ⅣB族的字母代号是D,
故答案为:ⅡA;ⅤA;D;
(3)周期表中8、9、10三列为Ⅷ族,则Ⅷ族元素指H、I、J三个纵列,
故答案为:H;I;J;
(4)S所在的格内包括15种元素,称为镧系元素,
故答案为:15;镧系;
(5)副族与Ⅷ统称为过渡元素,过渡元素区用粗线框表示为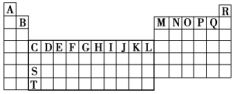 ,
,
故答案为: ;
;
(6)最外层8个电子的元素在0族,则最外层8个电子的元素在周期表的第R纵列,
故答案为:R.
点评 本题考查位置、结构与性质,为高频考点,把握周期表的结构、元素的位置为解答的关键,侧重分析与应用能力的考查,注意过渡元素的位置,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 陶瓷是硅酸盐产品 | B. | 葡萄糖可用于制镜业 | ||
| C. | 纸的主要成分为纤维素 | D. | 汉白玉的主要成分碳酸钙属于碱类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
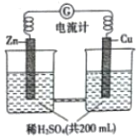 如图所示由锌片、铜片和稀H2SO4(密度为1.25g•cm-3)组成的原电池,一段时间后,若锌片只发生电化学反应,当在铜片上放出1.68L(标准状况下)气体时,H2SO4恰好梢耗一半,则原硫酸溶质的质量分数为( )
如图所示由锌片、铜片和稀H2SO4(密度为1.25g•cm-3)组成的原电池,一段时间后,若锌片只发生电化学反应,当在铜片上放出1.68L(标准状况下)气体时,H2SO4恰好梢耗一半,则原硫酸溶质的质量分数为( )| A. | 0.75% | B. | 2.94% | C. | 5.88% | D. | 11.76% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰醋酸、纯碱、明矾、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | 电解质是在水溶液或熔融状态下能导电的化合物 | |
| C. | 在含有1 mol Fe(OH)3的胶体中,含有NA个Fe(OH)3胶粒 | |
| D. | 玻璃棒在化学实验中只起到搅拌的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在熔融状态下不导电的化合物都是非电解质 | |
| B. | 液氯是纯净物,氯水是混合物,均不属于电解质 | |
| C. | SO2溶于水能导电,所以SO2是电解质 | |
| D. | 硫酸溶于水可以导电,所以浓硫酸是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
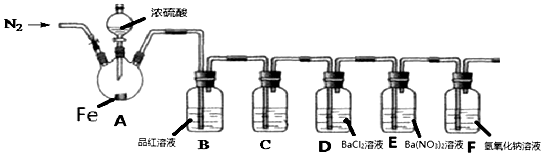
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com