
�ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�¶ȣ��棩 | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1����д����ҵ�ϳɰ��Ļ�ѧ����ʽ ��
�����ϱ����ݿ�֪�÷�ӦΪ���ȷ�Ӧ�������� ��
�������ϣ�Ϊ������ƽ��ʱH2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��������ţ�
a������ѹǿ b��ʹ�ú��ʵĴ���
c�������¶� d����ʱ����������е�NH3
��2��ԭ����H2��ͨ����Ӧ CH4(g) + H2O (g) CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е� 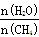 �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
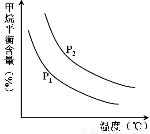
��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1 P2���>������=����<������
�ڸ÷�ӦΪ ��Ӧ������ȡ����ȡ�����
��3��ԭ����H2����ͨ����ӦCO(g) + H2O(g)  CO2 (g) + H2(g) ��ȡ��
CO2 (g) + H2(g) ��ȡ��
��T ��ʱ�����ݻ��̶�Ϊ5 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08 mol��L-1����ƽ��ʱCO��ת����Ϊ ���÷�Ӧƽ�ⳣ���ı���ʽΪ ��
�ڱ����¶���ΪT �棬�ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ������������з�Ӧ�����������ܹ�˵����ϵ����ƽ��״̬���� ������ţ���
a��������ѹǿ����ʱ��ı�
b�����������ܶȲ���ʱ��ı�
c����λʱ��������a mol CO2��ͬʱ����a mol H2
d���������n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 1 : 1 : 1
����11�֣�
��1���� N2 + 3H2  2 NH3��1�֣�
2 NH3��1�֣�
�� ���¶����ߣ���Ӧ��ƽ�ⳣ��K��С��1�֣��� a��d��2�֣�
��2�� �� <��1�֣� �� ���ȣ�1�֣�
��3�� �� 60 %��2�֣� K=c(CO2)c��H2��/c(CO)c(H2O)����1�֣�
�� c��2�֣�
��������
�����������1���ٹ�ҵ���õ����������ڸ��¸�ѹ�����������·�Ӧ���ɰ�������ѧ����ʽΪN2 + 3H2  2 NH3��
2 NH3��
���¶����ߣ�Kֵ��С��˵�������¶ȣ�ƽ�������ƶ���������Ӧ�Ƿ��ȷ�Ӧ��
��a.����ѹǿ��ƽ�������ƶ���������ת����������ȷ��b.ʹ�ô�����ֻ�ܼӿ췴Ӧ���ʣ����ܸı�ƽ�⣬����������ת���ʲ��䣬����c.�����¶ȣ�ƽ�������ȷ�Ӧ�����ƶ������������¶ȣ�ƽ�������ƶ���������ת���ʽ��ͣ�����d. ��ʱ����������е�NH3�����������Ũ�ȼ�С��ƽ�������ƶ���������ת����������ȷ����ѡad��
��2���ٸ��ݷ�Ӧ�Ļ�ѧ����ʽ��֪���¶�һ����ѹǿ����ƽ�������ƶ�������ĺ�����������P1<P2��
��ѹǿһ��ʱ���¶����ߣ������ƽ�⺬�����٣�˵�������¶ȣ�ƽ�������ƶ���������Ӧ�����ȷ�Ӧ��
��3����ƽ��ʱ��CO�ĵ�Ũ��Ϊ0.08 mol��L-1����ʼCO��Ũ����1mol/5L=0.2mol/L������ƽ��ʱC��ת�����ǣ�0.2-0.08��mol/L/0.2mol/L=60%������ƽ�ⳣ���Ķ��壬�÷�Ӧ��ƽ�ⳣ���ı���ʽΪK=c(CO2)c��H2��/c(CO)c(H2O)��
��a���÷�Ӧ���������ʵ�������Ŀ��淴Ӧ�����������ѹǿ�����״̬��һ����ƽ��״̬������b��������������䣬��������ܶ�ʼ�ղ��䣬���������ܶȲ����״̬��һ����ƽ��״̬������c����λʱ��������a mol CO2��ͬʱ����a mol H2���������淴Ӧ������ȵ���������ƽ��״̬����ȷ��d�����ݢ٣��ɼ���÷�Ӧ��ƽ�ⳣ��K= c(CO2)c��H2��/c(CO)c(H2O)=9/4���������n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 1 : 1 : 1ʱ��Qc= c(CO2)c��H2��/c(CO)c(H2O)=1�������ڸ��¶��µ�ƽ�ⳣ�������Բ���ƽ��״̬������ѡc��
���㣺���黯ѧƽ����ƶ���ƽ��״̬���жϣ�ƽ�ⳣ���ļ�����Ӧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ����и߶���ѧ�ڵ�����������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
Ksp(AgCl)��1.56��10��10 ��Ksp(AgBr)��7.7��10��13,Ksp(Ag2CrO4)��9.0��10��12 ,��֪��ij��Һ�к���C1-, Br- ��CrO42-��Ũ�Ⱦ�Ϊ0.010mo1��L-�������Һ����μ���0.010mol��L-1��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ
A��C1- ��Br-��CrO42- B��CrO42-��Br-��C1-
C��Br-��C1-��CrO42- D��Br- ��CrO42-��C1-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��̨�и�����ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ƻ����Ľṹ��ʽΪ ������˵����ȷ����
������˵����ȷ����
A��ƻ�������ܷ���������Ӧ�Ĺ�������2��
B��1 molƻ�������3 mol NaOH�����кͷ�Ӧ
C��1 molƻ��������������Na��Ӧ����1 mol H2
D��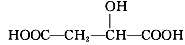 ��ƻ���ụΪͬ���칹��
��ƻ���ụΪͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У����ڷ�Ӧ��������Ũ�Ȳ���ı䷴Ӧ�������
A��CO2ͨ�����ʯ��ˮ�� B��Na2CO3��Һ�е���HCl��Һ
C�������м���п�� D����˿��������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ָ�������У����и�������һ���ܹ������������
A����pH=1����ɫ��Һ�У�SO42����Cu2+��Na+��Cl��
B��ʹpH��ֽ�ʺ�ɫ����Һ�У�Fe2+��NO3-��SO42-��Na+
C����c(H+)/c(OH��)= 1��1013����Һ�У�NH4+��Ca2+��C1����K+
D���������ۺ����������������Һ�У�NH4����Na����NO3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�±�ΪԪ�����ڱ���һ���֡������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣺

��1���ܢݢ�ԭ�Ӱ뾶��С�����˳��Ϊ(��Ԫ�ط��ű�ʾ) ��
�ڢۢߵ���ۺ����������������ǿ��˳����(�û�ѧʽ��ʾ) ��
��2������ݳ����¿ɷ�����Ӧ���ɻ�����A,���õ���ʽ��ʾA���γɹ���______________��
��3���ɱ���Ԫ�آ٢ۢܢޢ����γɵij�������X��Y��Z��M��N�ɷ������·�Ӧ��

��X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ ��
����N��ȡ��Ӧ�ĵ��������õķ����� ��
��M��Һ�����ԣ�ԭ����(�����ӷ���ʽ����) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ӦA(s)��2B(g)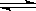 2C(g)��һ�ܱ������н��У����ı���������֮һʱ��һ��������Ӧ���ʵ���
2C(g)��һ�ܱ������н��У����ı���������֮һʱ��һ��������Ӧ���ʵ���
A������A���ʵ����� B�������¶�
C��ѹ����Ӧ������� D�����ĵ�����B����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йظ����ж�����������ȷ����
A��1molH2ȼ�շų�������ΪH2��ȼ����
B��Na2SO3��H2O2�ķ�ӦΪ������ԭ��Ӧ
C��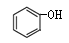 ��
��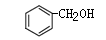 ��Ϊͬϵ��
��Ϊͬϵ��
D��BaSO4��ˮ��Һ�����磬��BaSO4���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(12��)�������б仯��ϵ��
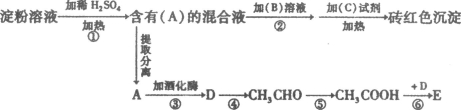
��֪��E��һ�־��й���ζ��������ˮ�����ʣ�����գ�
��1��A���ʵ�����______________________ ��
B��ҺΪ____________________________������Ϊ_________________________________��
��2��д���ܡ���������Ӧ�Ļ�ѧ����ʽ����( )���б�����Ӧ���͡�
�� _______________________________________________________ ( )
��_________________________________________________________ ( )
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com