
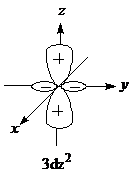
 ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.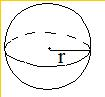 或
或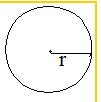 ,
, 或
或 ,以r为半径的球内1s电子出现的几率为90%;
,以r为半径的球内1s电子出现的几率为90%;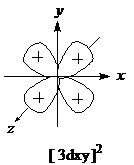 ,表示运动在3dxy原子轨道上电子出现的几率密度;
,表示运动在3dxy原子轨道上电子出现的几率密度; ,表示运动在3dxy原子轨道上电子出现的几率密度;
,表示运动在3dxy原子轨道上电子出现的几率密度; ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象. ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.


科目:高中化学 来源: 题型:
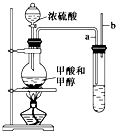 已知甲酸(HCOOH)是羧酸中组成最简单的酸,它具有羧酸的性质,在实验室里常用甲酸在浓硫酸的作用下制取少量一氧化碳,现用甲酸与甲醇反应制取甲酸甲酯来验证甲酸具有能发生酯化反应的性质,装置如图所示
已知甲酸(HCOOH)是羧酸中组成最简单的酸,它具有羧酸的性质,在实验室里常用甲酸在浓硫酸的作用下制取少量一氧化碳,现用甲酸与甲醇反应制取甲酸甲酯来验证甲酸具有能发生酯化反应的性质,装置如图所示查看答案和解析>>
科目:高中化学 来源: 题型:
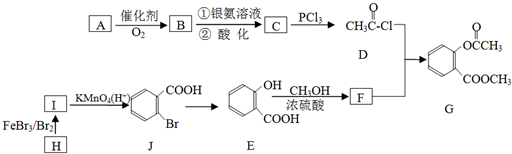
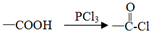
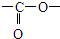 结构
结构查看答案和解析>>
科目:高中化学 来源: 题型:
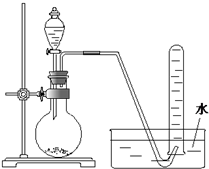
| A、用H2O2溶液和MnO2反应制取O2 |
| B、用浓盐酸和MnO2反应制取Cl2 |
| C、用稀硫酸与石灰石反应制取CO2 |
| D、用NH4Cl和Ca(OH)2反应制取NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
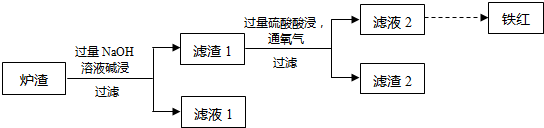
查看答案和解析>>
科目:高中化学 来源: 题型:
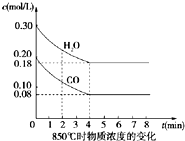 在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应:
在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com