
 ②H20
②H20 ③O=C=O
③O=C=O ④CCl4
④CCl4 ⑤Fe2+Fe2+⑥N2
⑤Fe2+Fe2+⑥N2
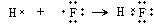 .
. 分析 先判断化合物类型及所含化学键类型,离子化合物由阳离子与银离子构成,阳离子电子式为阳离子符合,阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构,据此解答.
解答 解:①NaOH为离子化合物,电子式为
故答案为:
②水分子为共价化合物,氧原子分别与两个氢原子通过电子对共用形成共价键,电子式为:
故答案为:
③O=C=O为共价化合物,碳原子与两个氧原子分别共用两对电子,电子式为: ;
;
故答案为: ;
;
④四氯化碳为共价化合物,碳原子与四个氯原子分别共用1对电子,电子式;
故答案为:
⑤金属阳离子电子式为阳离子符号,所以二价铁离子电子式为:Fe2+;
故答案为:Fe2+;
⑥氮气为非金属单质,含有氮氮共价键,两个氮原子之间共用3对电子,电子式 ;
;
故答案为: ;
;
⑦HF为共价化合物,各原子满足8电子稳定结构,共价键形成过程为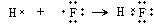
故答案为: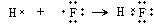
点评 本题考查了电子式的书写,明确物质所含化学键的类型及电子式书写应注意的问题是解题关键,注意金属阳离子电子式为其离子符号.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石和石墨互为同位素 | |
| C. | 石墨能量高于金刚石 | |
| D. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小:Na>S>O | B. | 稳定性:HI>HBr>HCl>HF | ||
| C. | 碱性强弱:KOH>Ca(0H)2>Mg(OH)2 | D. | 还原性强弱:I一>CI一>F? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最终三支试管的颜色各不相同 | |
| B. | A试管中Fe(OH)3含量最高 | |
| C. | 直接加热蒸发Fe2(SO4)3溶液可得到Fe2(SO4)3晶体 | |
| D. | B试管中Fe2(SO4)3不能发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式
的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式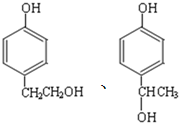 (其中之一).
(其中之一).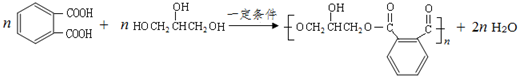 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜矿石在细菌作用下直接转换为单质铜,这个过程中叫做生物炼铜 | |
| B. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,相同条件下,某物质的热值越高,其标准燃烧越大 | |
| C. | 铅蓄电池是最常见的二次电池,可根据硫酸的密度来判断铅蓄电池是否需要充电 | |
| D. | “地沟油”禁止食用,但可以通过物理变化制肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
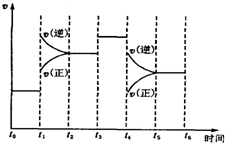 已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol.
已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol.| T/K | 473 | 573 | 673 | … |
| K | 4.4×10-2 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 碘元素的质子数为53 | |
| B. | 碘原子的质量数为126.9 | |
| C. | 碘原子核外有5种不同能量的电子 | |
| D. | 碘原子最外层有7种不同运动状态的电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com