
短周期元素甲、乙、丙、丁在元素周期表的相对位置如表所示,其中甲的气态氢化物的水溶液呈碱性,则下列判断正确的是双选) )。
| 甲 | 乙 | |
| 丙 | 丁 |
A.甲位于元素周期表中第二周期ⅤA族
B.原子半径:甲>乙
C.单质的氧化性:丙>乙
D.气态氢化物的稳定性:丁>丙>乙
科目:高中化学 来源: 题型:
1)估计下列各变化过程是熵增还是熵减。
①NH4NO3爆炸:2NH4NO3(s)===2N2(g)+4H2O(g)+O2(g)
②水煤气转化:CO(g)+H2O(g)===CO2(g)+H2(g)
③臭氧的生成:3O2(g)===2O3(g)
(2)可逆反应A(g)+B(g)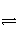
 2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如右图所示。
2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如右图所示。
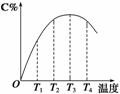
①由T1向T2变化时,正反应速率________逆反应速率。(填“>”、“<”或“=”)
②由T3向T4变化时,正反应速率________逆反应速率。(填“>”、“<”或“=”)
③反应在________温度下达到平衡。
④此反应的正反应为________热反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mo1·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度始终增大
B.c(NH4+) / c (NH3·H2O)先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
1)已知298 K时白磷、红磷完全燃烧的热化学方程式分别为P4s,白磷)+5O2g)===P4O10s)
ΔH1=-2 983.2 kJ·mol-1
Ps,红磷)+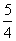 O2g)===
O2g)===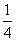 P4O10s)
P4O10s)
ΔH2=-738.5 kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式为
____________________________________________________。
2)已知298 K时白磷不完全燃烧的热化学方程式为P4s,白磷)+3O2g)===P4O6s)
ΔH=-1 638 kJ·mol-1。在某密闭容器中加入62 g白磷和50.4 L氧气标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________,反应过程中放出的热量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第ⅤA族,甲与丙同主族,丁原子最外层电子数与电子层数相等,则双选) )。
A.原子半径:丙>丁>乙
B.单质的还原性:丁>丙>甲
C.甲、乙、丙的氧化物均为共价化合物
D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学腐蚀与电化学腐蚀的说法中,错误的是
( )。
A.均是被腐蚀的金属失去电子的过程
B.均是需要有氧气参加的反应
C.化学腐蚀与电化学腐蚀往往是同时发生的
D.在无水环境中的腐蚀一般不属于电化学腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
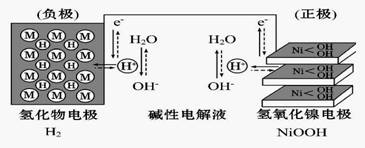
大功率的镍氢电池使用在油电混合动力车辆中。镍氢电池NiMH电池正极板材料为NiOOH,负极板材料为吸氢合金,下列关于该电池的说法中正确的的是
A. 放电时电池内部H+向负极移动
B. 充电时,将电池的负极与外接电源的正极相连
C. 充电时阳极反应为Ni(OH)2+ OH-- e-====NiOOH+H2O
D. 放电时负极的电极反应式为MHn-ne- = M+nH+
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.已知A、B、C、D四种分子所含原子的数目依次为1、3、6、6,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1:2。D是一种有毒的有机物。
(1)组成A分子的原子的元素符号是 ;(1分)
(2)从B分子的立体结构判断,该分子属于 分子(填“极性”或“非极性”);(1分)
(3)C分子中都包含_______个σ键,_______个π键;(2分,每空1分)
(4)D的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明D是何物质):
__________________________________________________ ____。(2分)
Ⅱ.CO的结构可表示为C≡O,N2的结构可表示为N≡N。
(5)下表是两者的键能数据:(单位:kJ/mol)
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
 结合数据说明CO比N2活泼的原因:________________________________
结合数据说明CO比N2活泼的原因:________________________________
___________________________________________________________。(2分)
Ⅲ.(6)基态Ni原子的核外电子排布式为 。(2分)
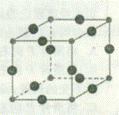
IV.(7)Cu3N的晶胞结构如右图,N3-的配位数为__________。(2分)
查看答案和解析>>
科目:高中化学 来源: 题型:
H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com