
分析 (1)将锌片和银片浸入稀硫酸中组成原电池,锌做负极,失电子发生氧化反应,银片做正极,溶液中氢离子在银电极得到电子发生还原反应;
(2)依据该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,分析判断电极质量减小为反应的锌的质量为13g,依据电极反应和电子守恒计算生成的气体物质的量得到气体体积和电子转移电子的物质的量.
解答 解:(1)将锌片和银片浸入稀硫酸中组成原电池,锌做负极,失电子发生氧化反应,电极反应为:Zn-2e-═Zn2+,银片做正极,溶液中氢离子在银电极得到电子发生还原反应,电极反应为:2H++2e-═H2↑,
故答案为:Zn-2e-═Zn2+;2H++2e-═H2↑;
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,分析可知电极质量减小的是负极反应的锌的质量,物质的量=$\frac{60g-47g}{65g/mol}$=0.2mol;
①锌做负极,失电子发生氧化反应,电极反应为:Zn-2e-═Zn2+,银片做正极,溶液中氢离子在银电极得到电子发生还原反应,电极反应为:2H++2e-═H2↑,依据电子守恒可知,转移电子物质的量为0.4mol,生成氢气物质的量为0.2mol,标准状况下体积=0.2mol×22.4L/mol=4.48L,
故答案为:4.48L;
②依据计算可知转移电子物质的量为0.4mol,故答案为:0.4mol.
点评 本题考查了原电池原理的分析判断,电极反应,电极名称,电子守恒的计算应用,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 干电池中锌筒为正极,石墨棒为负极 | |
| B. | 干电池长时间连续工作后,糊状物可能流出,腐蚀用电器 | |
| C. | 干电池工作时,电流方向是由锌筒经外电路流向石墨棒 | |
| D. | 干电池可实现化学能向电能和电能向化学能的相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化石燃料在燃烧过程中会产生污染环境的CO、SO2等有害气体 | |
| B. | 直接燃烧煤不如将煤进行深加工后再燃烧的效果好 | |
| C. | 太阳能、氢能、风能、核能、天然气等都属于新能源 | |
| D. | 水煤气是一种二次能源,比煤直接燃烧污染小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、甲苯、乙醇、乙酸都可以发生取代反应 | |
| B. | 能发生银镜反应的有机物都是醛 | |
| C. | 乙酸乙酯在无机酸或碱存在时都能发生水解反应 | |
| D. | 可用浓溴水来区分乙醇和苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
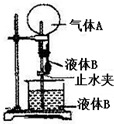 如图是实验室进行“喷泉”实验的一种装置,使用下列物质一定不会出现“喷泉”现象的是( )
如图是实验室进行“喷泉”实验的一种装置,使用下列物质一定不会出现“喷泉”现象的是( )| 选项 | 气体A | 液体B |
| A | HCl | 水 |
| B | SO2 | NaOH溶液 |
| C | Cl2 | 饱和食盐水 |
| D | NH3 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
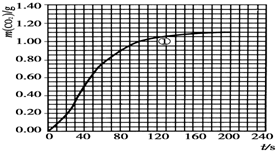 某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究大理石规格 (粗、细)对该反应速率 的影响. |
| ② | ||||
| ③ | ||||
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
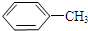 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$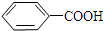
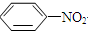 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$
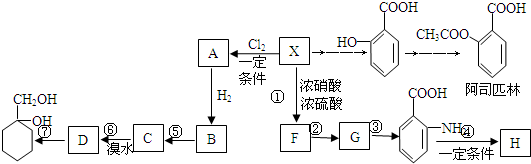
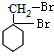 ,G
,G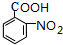 .
.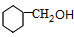 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$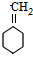 +H2O.
+H2O.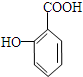 与碳酸氢钠溶液反应:
与碳酸氢钠溶液反应: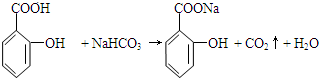 .
.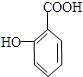 有多种同分异构体,其中属于芳香族化合物的同分异构体不可能为下列中的ad.
有多种同分异构体,其中属于芳香族化合物的同分异构体不可能为下列中的ad.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com