
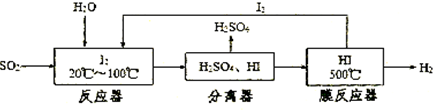
������FeS2��ȼ�ղ�����SO2ͨ�����й��չ��̼����Ƶ�H2SO4�������Ƶ�H2��
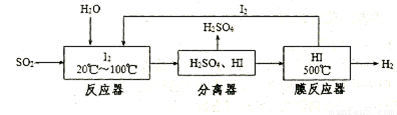
��1���ù�������ѭ�����õ�����Ϊ ��
��2���ڸù����У�ʹ��Ĥ��Ӧ����ʱ�����HI�ֽ������H2��Ŀ���� ����ƽ���ƶ���ԭ�����ͣ���
��3��ij�о���ѧϰС����̽��SO2�ܷ���BaCl2��Һ��Ӧ����BaSO3��������������ʵ�顣��֪Ũ����ķе�Ϊ338�棬����ʱ�Ƶƻ�����¶�Ϊ400�桫500�档
�ټ�ͬѧ��װ��I����ʵ�飬����BaCl2��Һ�г��ְ�ɫ�������Ұ�ɫ�������������ᣬ��������ɸð�ɫ�����Ŀ���ԭ�� �������ӷ���ʽ��ʾ����
����ͬѧ��Ϊ��ͬѧ��װ�ò����ƣ�����˸Ľ�װ��II����ʵ�飨�г�װ�ú�A�м���װ�����ԣ��������Ѽ�飩��
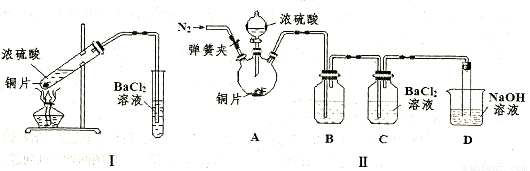
a�����ɼ�ͨ��N2��һ��ʱ���رյ��ɼУ�b���μ�һ����Ũ���ᣬ����A��һ��ʱ���C��δ���������ɡ�����a��Ŀ���� ��װ��B�еļ��� ��
�۱�ͬѧȡ��ʵ����C����Һ�������μ�һ����ɫ��Һ����������������İ�ɫ��������ͬѧ�μӵ��Լ������� ������ĸ��ţ���
a��NaOH��Һ b��H2O2��Һ c��������ˮ d������KmnO4��Һ
��װ��D���뵼�����ӵ���Ӳ�ʲ����ܣ���װ��D�������� ��
��1��I2 ��2�֣�
��2��ʹƽ��������Ӧ�����ƶ�����߲���IJ��ʡ���2�֣�
��3���� SO42����Ba2+=BaSO4����2Ba2+��2SO2��O2��2H2O=2BaSO4����4H+��2�֣����һ�������֣�
�� �ų�װ���е�O2��2�֣� ����NaHSO3��Һ��2�֣�
�� b��2�֣� ������β������������2�֣�
��������
�����������1���ɹ������̿�֪��ѭ�����õ�����ΪI2����2����ʱ�����HI�ֽ������H2��ʹHI�ķֽ�ƽ��������Ӧ�����ƶ��������I2 ��H2�IJ��ʡ���3����С������ץס��֪��Ϣ��Ũ����ķе�Ϊ338 �棬����ʱ�ƾ��ƻ�����¶�Ϊ400�桫500�桱��˵��Ũ�������¶Ƚϸ�ʱҲ�ܻӷ���H2SO4�������ٰ�ɫ����ӦΪBaSO4������ԭ���ж���һ�ǻӷ�����H2SO4�ṩ��SO42����Ba2+��Ӧ���ɣ����ǿ�����O2���������¡��ڲ���aͨ��N2Ŀ�����ų�װ���е�O2��C��δ���������ɣ�˵��B�е��Լ������ջӷ�����H2SO4�Ҳ������µ����ʣ���������SO2��Ӧ���ʸ��Լ�Ӧ�DZ���NaHSO3��Һ������ʵ����C�е���Һ������SO2�����в���������İ�ɫ����Ӧ��BaSO4���μ�һ����ɫ��Һ�� ֻ����H2O2��Һ����װ��D�������Ǽ�������δ��Ӧ��SO2��ֹ������Ⱦ�����ܷ�ֹNaOH��Һ������װ��C��Ӱ��ʵ������
���㣺���������о�SO2������Ϊ�����ʵ���⣬�漰��ѧƽ����ƶ�ԭ���Ŀ��顣


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
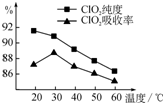 ij�о�С���û�����FeS2���������ƺ�������Һ��Ϸ�Ӧ�Ʊ�ClO2���壬����ˮ���ո�����ɵ�ClO2��Һ���ڴ˹�������Ҫ�������˵��¶ȣ����¶Ȳ���������Ӧ���ӣ�Ӱ������
ij�о�С���û�����FeS2���������ƺ�������Һ��Ϸ�Ӧ�Ʊ�ClO2���壬����ˮ���ո�����ɵ�ClO2��Һ���ڴ˹�������Ҫ�������˵��¶ȣ����¶Ȳ���������Ӧ���ӣ�Ӱ������- 3 |
2- 4 |
2- 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com