
| A、温度为298K时,pH<7 |
| B、c(CH3COOH)+c(CH3COO-)=0.1 mol?L-1 |
| C、c(CH3COOH)<c(CH3COO-) |
| D、c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |


科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
A、由-CH3、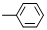 、-OH、-COOH四种原子团两两组合形成的有机物中,属于弱电解质的有4种 、-OH、-COOH四种原子团两两组合形成的有机物中,属于弱电解质的有4种 | ||
B、某种兴奋剂的结构简式如图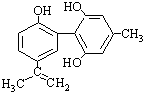 ,1mol该物质与浓溴水反应时最多消耗Br2为6mol ,1mol该物质与浓溴水反应时最多消耗Br2为6mol | ||
C、有机物X、Y、M的转化关系为:淀粉→X→Y
| ||
D、高分子化合物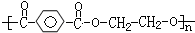 ,其链节为对苯二甲酸和乙二醇 ,其链节为对苯二甲酸和乙二醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
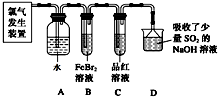
查看答案和解析>>
科目:高中化学 来源: 题型:
| A-B | A=B | C-B | C=B | |
| 键能:/kJ?mol-1 | 360 | 803 | 464 | 640 |
查看答案和解析>>
科目:高中化学 来源: 题型:
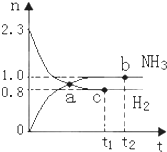 一定条件下,在绝热恒容2L密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)+Q,若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中一定正确的是( )
一定条件下,在绝热恒容2L密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)+Q,若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中一定正确的是( )| A、若在t2时刻再充入一定量He,达平衡时C(H2)<0.4mol/L |
| B、a点表示NH3生成速率与NH3分解速率相等 |
| C、b点和c点H2的转化率相等 |
| D、若在t1时刻再充入一定量H2,达平衡时化学平衡常数变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA |
| B、标况下,22.4L NO与11.2L O2混合后气体的分子数为2NA |
| C、标准状况下,22.4 L己烷中共价键数目为19NA |
| D、常温常压下,将0.1mol Fe投入足量的浓硝酸中,转移的电子数为0.3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com