
下列物质的转化在指定条件下能实现的是
A.Cu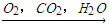 Cu2(OH)2CO3
Cu2(OH)2CO3  Cu(OH)2
Cu(OH)2
B.MgO 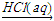 MgCl2(aq)
MgCl2(aq)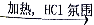 MgCl2(s)
MgCl2(s)
C.CaCl2(aq)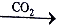 CaCO3
CaCO3  CaSiO3
CaSiO3
D.S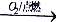 SO3
SO3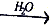 H2SO4
H2SO4
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2型分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L,W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A.原子半径:W>Z>Y>X>M
B.XZ2、M2Z2、W2Z2均为共价化合物
C.由X元素形成的单质不一定能导电
D.由Y、Z、M三种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:填空题
氮及其化合物与人类生产、生活息息相关.回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是__________,前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________。
(3)N2F2分子中N原子的杂化方式是__________,l mol N2F2含有__________molσ键.
(4)NF3的键角__________NH3的键角(填“<”“>”或“=”),原因是__________.
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4__________mol配位键.
(6)安全气囊的设计原理为6NaN3+FeIO3 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑
①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子__________.
②Na2O的晶胞结构如图所示,品胞边长为566pm,晶胞中氧原子的配位数为__________,Na2O晶体的密度为__________g•cm-3(只要求列算式,不必计算出结果)。

查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮训练三化学试卷(解析版) 题型:选择题
某温度下,向4.0 L恒容密闭容器中充入2.0 mol PCl5,反应PCl5(g) →PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
时间/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
下列说法正确的是
A.反应在前50 s的平均速率为v(PCl3)=0.0064 mol/(L·s)
B.若保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的△H﹤0
C.相同温度下,起始时向该容器中充入 4.0 mol PCl3、4.0 mol Cl2,达到平衡时,PCl3的转化率小于 80%
D.相同温度下,起始时向该容器中充入2.0 mol PCl5、0.40 mol PCl3和0.40 mol Cl2,达到平衡前v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:简答题
I.下列有关叙述正确的是( )
A.碱性锌锰电池中,MnO2是催化剂
B.银锌纽扣电池工作时,Ag2O被还原为Ag
C.放电时,铅酸蓄电池中硫酸浓度不断增大
D.电镀时,待镀的金属制品表面发生还原反应
II. 锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌.某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:

回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为______________。
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的______________操作.
(3)浸出液“净化”过程中加入的主要物质为______________,其作用是______________。
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气体是______________。
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质.“氧压酸浸”中发生的主要反应的离子方程式为______________。
(6)我国古代曾采用“火法”工艺冶炼锌.明代宋应星著《天工开物》中有关“升炼倭铅”的记载:“炉甘石十斤,装载入一尼罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火锻红,…,冷淀,毁罐取出,…即倭铅也.”该炼锌工艺主要反应的化学方程式为______________(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列物质与类别不对应的是
A | B | C | D |
小苏打
| 食用油
| 淀粉
| 84消毒液
|
盐 | 高分子化合物 | 糖类 | 混合物 |
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三第四次模拟理综化学试卷(解析版) 题型:选择题
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池的电池反应式为:NaMO2+nC?Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
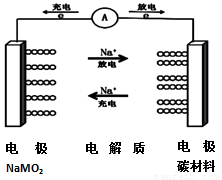
A.电池放电时,溶液中钠离子向负极移动
B.该电池负极的电极反应为:NaMO2-xe-═Na(1-x)MO2+xNa+
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.电池充电时的阳极反应式为:nC+x Na+-xe-═NaxCn
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
下列物质变化时,不需要破坏化学键的是( )
A.HCl溶于水 B.烧碱熔化 C.H2燃烧 D.I2升华
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:计算题
在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.08mol/L.
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若充入碘化氢0.4mol,求达到 平衡时碘化氢的转化率和氢气的物质的量浓度。2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com