
【题目】下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最慢的是 ( )
A. 10℃ 20mL 3mol/L的盐酸溶液 B. 10℃ 20mL 1mol/L的盐酸溶液
C. 20℃ 20mL 3mol/L的盐酸溶液 D. 20℃ 20mL 1mol/L的盐酸溶液
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列叙述错误的是
A. 活性炭具有除异味和杀菌作用
B. 高纯硅可用于制作光感电池
C. 中国天眼FAST用到的碳化硅是一种新型的无机非金属材料
D. 碘酒可用于皮肤外用消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气: 2NO+2CO ![]() 2CO2+N2 .
2CO2+N2 .
(1)写出CO2的结构式 , N2的电子式 .
(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示: 
①则反应速率 ![]() (a)、
(a)、 ![]() (b)、
(b)、 ![]() (c)的大小关系是;
(c)的大小关系是;
②下列可说明反应到达图中c点的是;
A.NO、CO、CO2、N2的浓度比值保持2:2:2:1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
D.容器中的气体质量或物质的量保持不变
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究. 【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
实验编号 | 实验目的 | T/℃ | NO初始浓度 | CO初始浓度 | 同种催化剂的比表面积 | 达平衡时所用的时间min |
Ⅰ | 参照实验 | 280 | 6.50×10﹣3 | 4.00×10﹣3 | 80 | t |
Ⅱ | 280 | 6.50×10﹣3 | 4.00×10﹣3 | 120 | 0.5t | |
Ⅲ | 360 | 6.50×10﹣3 | 4.00×10﹣3 | 80 | 0.2t |
【结论】①实验编号Ⅱ的实验目的为 .
②课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是 , 且反应速率将 . (填“增大”、“减小”、“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表的一部分,请回答心里问题: 
(1)若①和⑤可以形成原子个数比1:1的化合物,此时①显价.①和⑧形成的化合物的电子式为 .
(2)②和③的最高价含氧酸的酸性强弱顺序>(填分子式).
(3)④和⑦形成的常见化合物的晶体类型为 , 微粒间通过形成了该晶体.④和②形成的常见化合物的晶体类型为 , 微粒间通过形成了该晶体.
(4)⑥为材料的容器可以装运浓硫酸或浓硝酸的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 淀粉、纤维素、蛋白质和油脂都是天然的高分子化合物
B. 糖类是碳和水结合而成的化合物,故也称为“碳水化合物”
C. 糖类物质都可以水解
D. 油和脂肪都属于酯类,油中含有碳碳双键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: 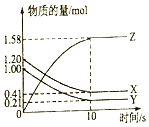
(1)反应的化学方程式为 .
(2)反应010s的化学反应速率v(Z)= .
(3)反应开始到10s,X的物质的量浓度减少了 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 向Al2(SO4)3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓
B. 向Fe(OH)3胶体中加入氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O
C. 将NaClO溶液与亚硫酸钠溶液混合:ClO-+SO32-=SO42-+Cl-
D. 用石墨作电极电解氯化镁溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法错误的是
A. 5NH4NO3![]() 2HNO3+4N2↑+9H2O的反应中,生成28gN2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O的反应中,生成28gN2,转移的电子数目为3.75NA
B. 常温常压下,7.8gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8NA
C. 若lL0.2mol/L的FeCl3溶液完全水解形成胶体,则胶体粒子数小于0.2NA
D. 标况下22. 4L NO和11.2L O2混合后所得气体分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com