
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:阅读理解
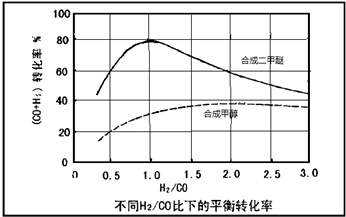
| 反应过程 | 化学方程式 | △H(kJ?mol-1) |
| 甲醇合成反应 | 2H2(g)+CO(g)=CH3OH(g) | -90.8 |
| 水煤气变换反应 | CO(g)+H2O(g)═CO2(g)+H2(g) | -41.3 |
| 甲醇脱水反应 | 2CH3OH(g)=CH3OCH3(g)+H2O(g) | -23.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃煤时应将块煤粉碎或磨成粉末 | B、燃煤时应通入足量的空气,且越多越好 | C、将煤制成水煤气 | D、将煤经过处理制成甲醇等 |
查看答案和解析>>
科目:高中化学 来源:2012年沪科版高中化学5.1从黑火药到酸雨练习卷(解析版) 题型:填空题
硫的氧化物(SO2和SO3)和大气污染
1)主要来源:煤炭燃烧、火山喷发等。
2)主要危害:产生 。有关的化学方程式是
3)减少污染物的原理和方法:
a.改善燃煤质量。降低煤的含硫量和含灰量。
b.改进燃烧装置和燃烧技术。如向煤中加入石灰石或生石灰,减少产物中SO2的含量,有关的化学方程式是 。
c.发展洁净煤技术。如煤的气化和液化,将焦炭在高温下与水蒸气反应,生成CO和H2;关的化学方程式是 。
d.开发洁净能源
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学必修二第四章 化学与可持续发展练习卷(解析版) 题型:选择题
我国的能源消耗以煤为主。据估计,全世界的煤炭最多供应200~300年。下列是关于利用煤炭资源的某些观点,其中论述正确的是( )
①直接燃煤虽然带来了污染问题,但同时提供了能量,污染与经济效益相比,经济效益更重要②人类在开发资源时,既要满足自身需要又不能以危害子孙后代为代价是杞人忧天④发展洁煤技术,提高燃煤效率,进行煤的干馏,可以提高煤的实用价值
A.①④ B.②③ C.①② D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com