
【题目】工业上利用甲苯制备一种芳香六元环酯(己)的方法如下:
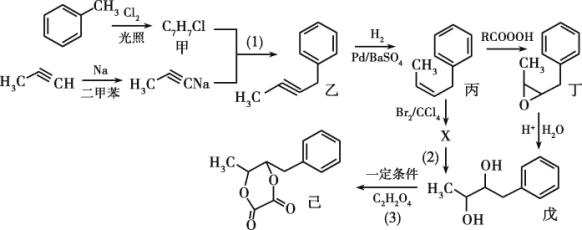
回答下列问题:
(1)写出物质丁的分子式_______,1mol丁完全燃烧需要氧气的物质的量为_______。
(2)物质甲的官能团名称为________。物质丙分子中共面的原子个数最多为_______。
(3)反应(3)的反应类型是_____,写出反应(1)的化学方程式_______。
(4)物质X的结构简式为______。
(5)物质丁的同分异构体较多,满足下列条件的物质丁的同分异构体数目是______,其中核磁共振氢谱有5组吸收峰,且峰面积之比为6:2:2:1:1的结构简式为______。
①能发生银镜反应 ②苯环上只有两个对位取代基
(6)写出以CH3CH=CH2为原料合成2-羟基丙酸(![]() )的合成路线(其他无机试剂任选)______。
)的合成路线(其他无机试剂任选)______。
【答案】C10H12O 12.5 mol 氯原子 18 酯化反应或取代反应 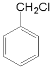 +
+![]()
![]()
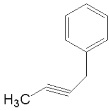 +NaCl
+NaCl 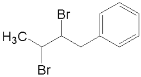 5
5 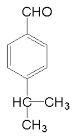

【解析】
根据题干合成路线可知,甲苯光照条件下与氯气发生甲基上的取代反应生成甲(C7H7Cl),则甲为 ,
,![]() 与Na反应生成丙炔钠(
与Na反应生成丙炔钠(![]() ),
),![]() 再与甲发生取代反应生成乙,乙与氢气发生碳碳三键的加成反应生成丙,丙与Br2的CCl4溶液发生碳碳双键的加成反应生成X,则X为
再与甲发生取代反应生成乙,乙与氢气发生碳碳三键的加成反应生成丙,丙与Br2的CCl4溶液发生碳碳双键的加成反应生成X,则X为 ,X水解生成戊,丙与RCOOOH发生氧化反应生成丁,丁酸化后生成戊,戊在一定条件下与C2H2O4反应得到己,据此分析解答。
,X水解生成戊,丙与RCOOOH发生氧化反应生成丁,丁酸化后生成戊,戊在一定条件下与C2H2O4反应得到己,据此分析解答。
(1)根据丁的结构简式可知,一个丁分子中含有10个C原子,12个H原子,1个O原子,则丁的分子式为C10H12O,丁在氧气中燃烧的化学方程式为2C10H12O+25O2→20CO2+12H2O,则1mol丁完全燃烧需要氧气的物质的量为12.5mol;
(2)根据上述分析,甲为 ,其官能团名称为氯原子,丙的结构简式为
,其官能团名称为氯原子,丙的结构简式为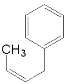 ,由于苯环上的所有原子共平面,与碳碳双键的所有原子共平面,甲基中最多3个原子共平面,则丙分子中最多有18个原子共平面;
,由于苯环上的所有原子共平面,与碳碳双键的所有原子共平面,甲基中最多3个原子共平面,则丙分子中最多有18个原子共平面;
(3)反应(3)为戊在一定条件下与C2H2O4发生酯化反应反应得到己,反应(1)为![]() 再与甲发生取代反应生成乙,反应的化学方程式为
再与甲发生取代反应生成乙,反应的化学方程式为 +
+![]()
![]()
 +NaCl;
+NaCl;
(4)根据上述分析可知,X为 ;
;
(5)物质丁的分子式为C10H12O,其同分异构体能够发生银镜反应,则含有醛基,且其苯环上只有两个对位取代基,则该同分异构体有 、
、 、
、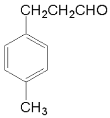 、
、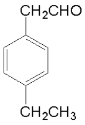 、
、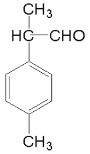 共5种,其中核磁共振氢谱有5组吸收峰,且峰面积之比为6:2:2:1:1的结构简式为
共5种,其中核磁共振氢谱有5组吸收峰,且峰面积之比为6:2:2:1:1的结构简式为 ;
;
(6)结合题干合成路线可知,以CH3CH=CH2为原料合成2-羟基丙酸(![]() )的合成路线可以为
)的合成路线可以为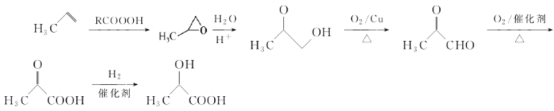 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某化学课外小组用图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。

(1)写出A中反应的化学方程式_______________。
(2)观察到A中的现象是_____________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式______________________________。
(4)C中盛放CCl4的作用是________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
①![]() ②
②![]() ③(CH3)3C—CHBr2 ④CHCl2—CHBr2 ⑤
③(CH3)3C—CHBr2 ④CHCl2—CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A. ①③⑥B. ②③⑤C. ②④D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,矩形OABC中,OA、OC分别在平面直角坐标系x轴、y轴的正半轴上,点D在AB上,将△CDB沿着CD翻折,点B恰好落在OA的中点E处,若四边形OCDA的面积为![]() ,则直线ED的解析式为( )
,则直线ED的解析式为( )
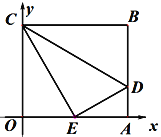
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 在医药合成中有着广泛的用途。下列有关该物质的说法正确的( )
在医药合成中有着广泛的用途。下列有关该物质的说法正确的( )
A.该化合物中含氧官能团为酯基
B.该化合物中的所有碳原子一定处于同一平面内
C.该化合物可发生取代反应、加成反应和氧化反应
D.该化合物的同分异构体中,苯环上有两个取代基的共3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH4+、Ba2+、Na+、H+、SO42-、NO3-、OH-、CO32-。将这四种溶液分别标记为A、B、C、D,进行如下实验:①在A或D中滴入C,均有沉淀生成;②D和B反应生成的气体能被A吸收;③A和D反应生成的气体能被B吸收。试回答下列问题:
(1)D的化学式是________,判断理由是_________________________________。
(2)写出相应物质的化学式:A___________,C___________。
(3)写出实验②中有关反应的离子方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是一种重要的化工产品。
(1)标准状况下,1 mol NH3的体积约为________L。
(2)实验室制取NH3的化学方程式为______________。
(3)收集NH3应使用________法,要得到干燥的NH3可选用___做干燥剂。
(4)压强对合成氨反应具有重要的影响。下表是反应达到平衡时压强与 NH3 含量的一些实验数据:
压强MPa | 10 | 20 | 30 | 60 | 100 |
NH3含量(体积分数%) | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
从表中数据可以推断:随着压强增大,平衡时NH3含量随之___(填字母)。
A.增大 B.减小 C.先增大再减小 D.不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用冶铅废渣(含Pb、PbO、PbS及Zn、Fe、Cu等杂质)制取立德粉和回收铅的工艺流程如下:
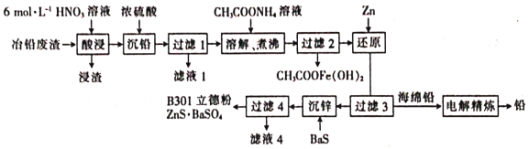
(1)“酸浸”时,PbS被氧化生成S,硝酸被还原为NO,则氧化0.3 mol PbS时,消耗HNO3______mol。
(2)“溶解、煮沸”时会发生多个反应。
①PbSO4溶解的离子方程式为__________________。(已知:Pb(CH3COO)2是弱电解质)
②“沉铅”时生成的沉淀中混有Fe3+,煮沸时醋酸铁水解的化学方程式为__________________。
(3)海绵铅(含少量Zn、Cu等杂质)进行“电解精炼”时,用PbSiF6、H2SiF6的混合溶液作电解液,海绵铅作_____(填“阳”或“阴”)极,阳极泥的主要成分是______(填化学式)。
(4)B301立德粉(ZnS·BaSO4)中ZnS的理论含量为29.4%。
①若要生产ZnS的理论含量为62.5%的B311高ZnS立德粉,可用的原料除BaS外,另两种原料可能为______。(填标号)
A. ZnSO4 B.NaCl C. ZnCl2 D. Na2SO4
②测定立德粉中ZnS的含量常用酸溶,调节pH至1~3,然后滴定形成K2Zn3[Fe(CN)6]2沉淀,该沉淀的溶度积常数Ksp的表达式为______。
(5)滤液4经加热后可返回______工序循环使用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com