
【题目】常温下用NaOH溶液滴定H2C2O4溶液的过程中,溶液中一lg![]() 和一lgc(HC2O42-)[或-lg
和一lgc(HC2O42-)[或-lg![]() 和-1gc(C2O42-)]的关系如图所示。下列说法正确的是
和-1gc(C2O42-)]的关系如图所示。下列说法正确的是
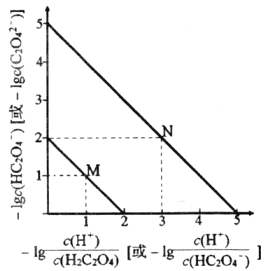
A. Ka1(H2C2O4)数量级为10-1
B. 曲线N表示-lg![]() 和-lg c(HC2O4-)的关系
和-lg c(HC2O4-)的关系
C. 向NaHC2O4溶液中加NaOH至c(HC2O4-)和c(C2O42-)相等,此时溶液pH约为5
D. 在NaHC2O4溶液中C(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
科目:高中化学 来源: 题型:
【题目】请回答下列关于有机物的问题:
(1)下列有机物属于酯类的是_________(填正确答案编号)。
A. ![]() B.
B. ![]() C.
C. ![]() D.CH3CH2OH
D.CH3CH2OH
(2)下列有机物不能发生水解反应的是__________(填正确答案编号)
A.油脂 B.葡萄糖 C.纤维素 D.蛋白质
(3)下列有机物属于芳香族化合物的是____(填正确答案编号,下同),与环己烷互为同系物的是_____,能使溴的四氯化碳溶液褪色的是___________;D和H2反应的化学方程式是____________。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C和甲、乙、丙均是由短周期元素形成的物质,D是过渡元素形成的常见单质,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)
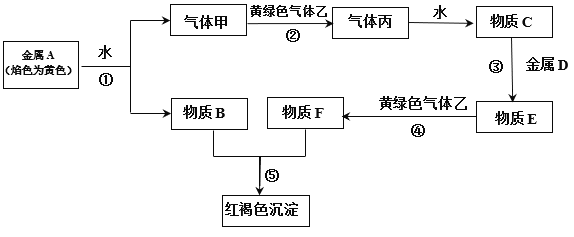
请回答下列问题:
(1)丙的电子式为_____;组成气体乙的元素在周期表的位置____;物质B含有的化学键类型是______;
(2)写出下列反应的离子方程式:
④ _________________________;
⑤ _____________________;
(3)金属D与稀硝酸反应,产生标准状况下1.12L的NO气体,则参加反应的硝酸为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中可逆反应 mA(g)+nB(g)![]() pC(g)+qQ(g)m、n、p、q为任意整数时,达到平衡的标志是
pC(g)+qQ(g)m、n、p、q为任意整数时,达到平衡的标志是
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变 ④各组分的质量分数不再改变 ⑤反应速率v(A)∶v(B)∶v(C)∶v(Q)=m∶n∶p∶q ⑥单位时间内m mol A断键反应,同时p mol C也断键反应
A. ③④⑤⑥ B. ①③④⑤ C. ②③④⑥ D. ①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型镁-锂双离子二次电池如图,下列关于该电池的说法不正确的是

A. 放电时,Li+由左向右移动
B. 放电时,正极的电极反应式为Li1-xFePO4+xLi++xe-= LiFePO4
C. 充电时,外加电源的正极与Y相连
D. 充电时,导线上每通过1mol e-,左室溶液质量减轻12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.二氧化氯是高效、低毒的消毒剂。已知:ClO2是极易溶于水的气体,实验室制备及性质探究装置如下图所示。回答下列问题:
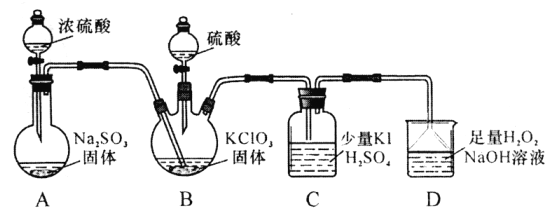
(1)置B用于制备ClO2,同时还生成一种酸式盐,该反应的化学方程式为___________。装置C中滴有几滴淀粉溶液,反应时有蓝色岀现。淀粉的作用是___________。
(2)C装置的导管靠近而不接触液面,其目的是_________________________________。
(3)用ClO2消毒自来水,其效果是同质量氯气的___________倍(保留一位小数)
(4)装置D用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2︰1,则还原产物的化学式是___________。
(5)若将C裝置中的溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:CO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:_________________________________。
②请设计实验证明你的假设(仅用离子方程式表示):______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应 CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
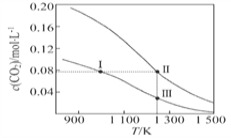
A. 反应 CO2(g)+C(s)![]() 2CO(g)的 ΔS>0、ΔH<0
2CO(g)的 ΔS>0、ΔH<0
B. 体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C. 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D. 逆反应速率v逆::v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g) ![]() S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如下图所示,下列说法正确的是( )
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如下图所示,下列说法正确的是( )
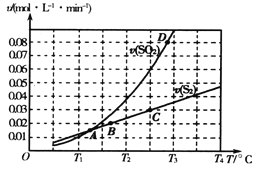
A. C点时达到平衡状态
B. 该反应的H>0
C. 增加C的量能够增大SO2的转化率
D. T3时增大压强,能增大活化分子百分数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com