
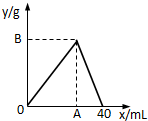
 如图是表示往50mL AlCl3溶液中滴加4mol?L-1的NaOH溶液,生成沉淀的质量(y轴)与消耗NaOH溶液的体积(x轴)的关系.填空:
如图是表示往50mL AlCl3溶液中滴加4mol?L-1的NaOH溶液,生成沉淀的质量(y轴)与消耗NaOH溶液的体积(x轴)的关系.填空:| 3 |
| 4 |
| (0.03×4)mol×1mol |
| 3mol×0.05mol |
| 1.56g |
| 78g/mol |
| 0.06mol |
| 4mol/L |
| 0.08mol |
| 4mol/L |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| PCI3 |
| △ |
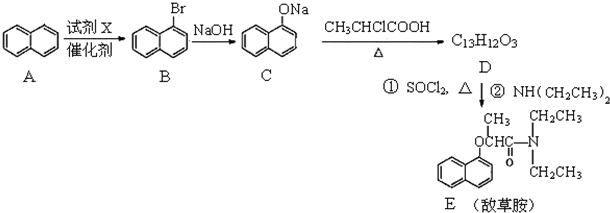
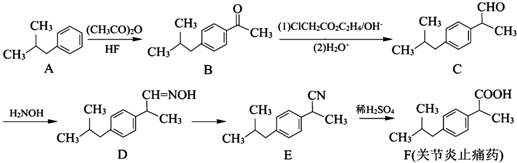
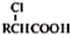 ,写出以苯酚、乙醇和乙酸为原料制备
,写出以苯酚、乙醇和乙酸为原料制备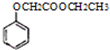 的合成路线流程图(无机试剂任用).合成路线流程图例如下:
的合成路线流程图(无机试剂任用).合成路线流程图例如下:| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
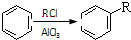 ②
②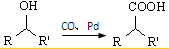 (R、R′表示烃基)
(R、R′表示烃基)| HBr |
| NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
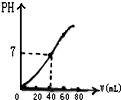 用1.0mol?L-1NaOH溶液中和某浓度H2SO4溶液,其PH和所用NaOH溶液的体积关系如图所示,则原H2SO4溶液的物质的量浓度和完全反应后溶液的大致体积是( )
用1.0mol?L-1NaOH溶液中和某浓度H2SO4溶液,其PH和所用NaOH溶液的体积关系如图所示,则原H2SO4溶液的物质的量浓度和完全反应后溶液的大致体积是( )| A、1.0mol?L-1、60mL |
| B、0.5mol?L-1、80mL |
| C、0.5mol?L-1、40mL |
| D、1.0mol?L-1、80mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2溶液和Na2CO3溶液 |
| B、稀盐酸和AgNO3溶液 |
| C、NaOH溶液和Al2(SO4)3溶液 |
| D、Ba(OH)2溶液和Na2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用铜片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面出现一层铜 |
| C、用铜作阳极,电解FeCl3溶液,在阴极上可析出铜 |
| D、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ag2O+H2O2═Ag+O2↑+H2O |
| B、H2O2═H2O+O2↑ |
| C、H2O2+Cr2(SO4)3+KOH═K2CrO4+K2SO4+H2O |
| D、Na2O2+HCl═H2O2+NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com