
”¾ĢāÄæ”æĻĀĮŠŠŌÖŹĢåĻÖĮĖ½šŹōĶØŠŌµÄŹĒ(””””)
A. Ņų²»Ņ×ÉśŠā B. Ģś³£ĪĀĻĀ²»ČÜÓŚÅØĻõĖį
C. ÄĘÓėĖ®¾ēĮŅ·“Ó¦·Å³öĒāĘų D. ½šŹō¾ßÓŠĮ¼ŗƵÄŃÓÕ¹ŠŌ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢś»ĘŹĒŅ»ÖÖÖŲŅŖµÄŃÕĮĻ£¬»ÆѧŹ½ĪŖFe2O3xH2O£¬¹ć·ŗÓĆÓŚĶæĮĻ”¢Ļš½ŗ”¢ĖÜĮĻ”¢ĪĽĢÓĆĘ·µČ¹¤Ņµ”£ŹµŃéŹŅÄ£Äā¹¤ŅµĄūÓĆĮņĖįŌü(ŗ¬Fe2O3¼°ÉŁĮæµÄCaO”¢MgOµČ) ŗĶ»ĘĢśæó·Ū(Ö÷ŅŖ³É·ÖĪŖFeS2) ÖʱøĢś»ĘµÄĮ÷³ĢČēĻĀ”£
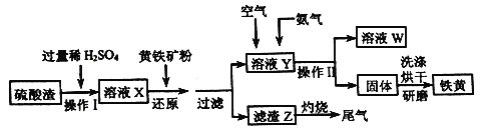
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©²Ł×÷IÖŠĪŖĮĖĢįøßĮņĖįŌüµÄČܽāĖŁĀŹ£¬æɲÉČ”µÄ“ėŹ©ÓŠ_________(“šĮ½Ģõ¼“æÉ)”£
£Ø2£©ČÜŅŗXÖŠŗ¬ÓŠµÄ½šŹōĄė×ÓÓŠFe3+ŗĶ_____£»ČÜŅŗXÖŠ¼ÓČė»ĘĢśæó·Ūŗó£¬ĻČ·¢Éś·“Ó¦FeS2+H2SO4( Ļ”)=FeSO4+ H2S”ü+S”ż£¬H2S ŌŁ½«Fe3+»¹Ō£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ_________”£
£Ø3£©ŌŚČÜŅŗY ÖŠĶØČėæÕĘųµÄÄæµÄŹĒ______________£¬ŌŁĶØČėNH3ŗóæɹŪ²ģµ½µÄĻÖĻóŹĒ__________£¬ČōĶØČėNH3ŗóČÜŅŗµÄpH ¹żøߣ¬»įÓ°Ļģ²śĘ·“æ¶Č£¬ŌŅņŹĒ_________”£
£Ø4£©²Ł×÷IIÖŠ³żÓƵ½²£Į§°ōĶā£¬»¹ŠčŅŖµÄ²£Į§ŅĒĘ÷ŹĒ________”£
£Ø5£©Čō½«ĀĖŌüZ×ĘÉÕ²śÉśµÄĪ²ĘųĶØČėČÜŅŗX ÖŠ£¬³ä·Ö·“Ó¦ŗóČÜŅŗµÄpH____(Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
£Ø6£©ĪŖĮĖ²ā¶ØĖłÖʱøĢś»ĘFe2O3xH2OÖŠxµÄÖµ£¬ÓĆ·ÖĪöĢģĘ½×¼Č·³ĘĮæm1gѳʷÖĆÓŚŪįŪöÖŠ¼ÓČČ”¢ĄäČ“ŗó³ĘĮ棻¾¹żÖŲø“²Ł×÷£¬µ±“ļµ½ŗćÖŲŹ±£¬²ŠĮō¹ĢĢåÖŹĮæĪŖm2g£¬Ōņx =______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æN”¢P”¢AsµÄ»ÆŗĻĪļŌŚŃŠ¾æŗĶÉś²śÖŠÓŠŠķ¶ąÖŲŅŖÓĆĶ¾”£
(1)»łĢ¬AsŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ_________”£
(2)NµÄµŚŅ»µēĄėÄܱČO“ó£¬ŌŅņŹĒ______________”£
(3)NH4+ÖŠH-N-HµÄ¼ü½Ē±ČNH3ÖŠH-N-H µÄ¼ü½Ē_______(Ģī”°“ó”±»ņ”°Š””±)£¬ŌŅņŹĒ____________”£
(4)K3AsO4ÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶ°üĄØ________£»AsO43- µÄæռ乹ŠĶĪŖ______”£As4O6µÄ·Ö×Ó½į¹¹ČēĶ¼1ĖłŹ¾£¬ŌņøĆ»ÆŗĻĪļÖŠAsµÄŌӻƷ½Ź½ŹĒ__________”£
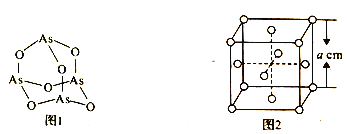
(5)»ÆŗĻĪļNH5ÖŠµÄĖłÓŠŌ×Ó×īĶā²ć¶¼Āś×ćĪČ¶Ø½į¹¹£¬ŌņNH5 ŹĒ_______¾§Ģ唣
(6)°×Į×(P4)µÄ¾§ĢåŹōÓŚ·Ö×Ó¾§Ģ壬Ę侧°ū½į¹¹ČēĶ¼2 (Š”Ō²Č¦±ķŹ¾°×Į×·Ö×Ó)”£ŅŃÖŖ¾§°ūµÄ±ß³¤ĪŖacm£¬°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµĪŖNA£¬ŌņøĆ¾§°ūÖŠŗ¬ÓŠP Ō×ÓµÄøöŹżĪŖ______£¬øĆ¾§ĢåµÄĆܶČĪŖ_________(ÓĆŗ¬NA”¢a µÄ“śŹżŹ½±ķŹ¾) g.cm-3”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒÓÉ4øöŌ²Ėł¹¹³ÉµÄŌŖĖŲøÅÄīµÄ¹ŲĻµĶ¼£¬ĘäÖŠ4ĪŖ×ī“óŌ²£¬3”¢2”¢1ŅĄ“Ī¼õŠ””£ŹŌÅŠ¶Ļ·ūŗĻÕāÖÖ¹ŲĻµµÄŹĒ

A. 1£®×ī»ł±¾ŌŖĖŲ”¢2£®»ł±¾ŌŖĖŲ”¢3£®Ö÷ŅŖŌŖĖŲ”¢4£®“óĮæŌŖĖŲ
B. 1£®“óĮæŌŖĖŲ”¢2£®Ö÷ŅŖŌŖĖŲ”¢3£®»ł±¾ŌŖĖŲ”¢4£®×ī»ł±¾ŌŖĖŲ
C. 1£®»ł±¾ŌŖĖŲ”¢2£®×ī»ł±¾ŌŖĖŲ”¢3£®“óĮæŌŖĖŲ”¢4£®Ö÷ŅŖŌŖĖŲ
D. 1£®Ö÷ŅŖŌŖĖŲ”¢2£®“óĮæŌŖĖŲ”¢3£®×ī»ł±¾ŌŖĖŲ”¢4£®»ł±¾ŌŖĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻć½¶¹ūŹµ³ÉŹģ¹ż³ĢÖŠÓÉÓŚ“¢“ęµÄĪļÖŹ±äĪŖæÉČÜŠŌĢĒ“Ó¶ųŹ¹¹ūŹµĢš¶ČŌö¼Ó”£Ä³ŠĖȤŠ”×é¶Ō“ĖÉśĄķ±ä»Æ½ųŠŠĮĖ³õ²½Ģ½¾æ£ŗČ”Ī“³ÉŹģĻć½¶¹ūŹµČōøÉ·ÅŌŚŹŹŅĖĢõ¼žĻĀČĆĘä×ŌČ»³ÉŹģ£¬ĆæĢģ¶ØŹ±Č”10 g¹ūČāŃŠÄ„ÅäÖĘ³É100 mL“ż²āŃłŅŗĘ½·ÖĪŖA”¢BĮ½·Ż£¬·Ö±šÓƵāŅŗŗĶģ³ĮÖŹŌ¼Į¼ģ²ā£¬¼ĒĀ¼ŃÕÉ«ÉīĒ³µÄ±ä»Æ”£
(1)ŃłŅŗAÓƵāŅŗ¼ģ²āµÄÄæµÄŹĒ__________________£»ŃłŅŗBÓĆģ³ĮÖŹŌ¼Į¼ģ²āµÄÄæµÄŹĒ___________”£
(2)ģ³ĮÖŹŌ¼ĮŹ¹ÓĆŹ±Šč¼×”¢ŅŅŅŗµČĮæ»ģŗĻ¾łŌČŗóŌŁ×¢Čė£¬²¢____________¹Ū²ģŃÕÉ«±ä»Æ”£
(3)øł¾ŻŌ¤ĘŚ½į¹ūŌŚ×ų±źĶ¼ÖŠ»³öĮ½ÖÖŃÕÉ«µÄ±ä»Æ”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ
A. H2SO4µÄĦ¶ūÖŹĮæŹĒ98
B. µČÖŹĮæµÄO2ŗĶO3ÖŠĖłŗ¬µÄŃõŌ×ÓŹżĻąĶ¬
C. µČÖŹĮæµÄCOÓėCO2ÖŠĖłŗ¬Ģ¼Ō×ÓŹżÖ®±ČĪŖ7©U11
D. 98g H2SO4ČܽāÓŚ500mLĖ®ÖŠ£¬ĖłµĆČÜŅŗÖŠĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ2 mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĮŠŹĀŹµ£¬Ķź³ÉĻą¹ŲµÄĄė×Ó·½³ĢŹ½»ņ»ÆѧŹ½£¬±ŲŅŖŹ±æɼÓŅ»¶ØĪÄ×ÖĖµĆ÷£ŗ
£Ø1£©ĮņĖįĀĮ¼Ų[Ć÷·ÆKAl£ØSO4£©2”¤12H2O]æÉŅŌ×÷¾»Ė®¼Į_____________________”£
£Ø2£©ÅŻÄĆš»šĘ÷µÄ»ÆѧŌĄķ________________________________________________”£
£Ø3£©Čȵēæ¼īČÜŅŗĒåĻ“ÓĶĪŪ___________________________________________”£
£Ø4£©¼ÓČČÕōøÉFeCl2Ė®ČÜŅŗ²¢×ĘÉÕ£¬µĆµ½ĪļÖŹµÄ»ÆѧŹ½ĪŖ___________”£
”¾“š°ø”æ Al3++3H2O![]() Al(OH)3£Ø½ŗĢ壩+3H+ Al3++3HCO3-=Al(OH)3”ż+3CO2”ü CO32-+H2O
Al(OH)3£Ø½ŗĢ壩+3H+ Al3++3HCO3-=Al(OH)3”ż+3CO2”ü CO32-+H2O![]() HCO3-+OH-£¬¼ÓČČæÉŅŌ“Ł½ųĖ®½ā£¬ČÜŅŗ¼īŠŌŌöĒæ Fe2O3
HCO3-+OH-£¬¼ÓČČæÉŅŌ“Ł½ųĖ®½ā£¬ČÜŅŗ¼īŠŌŌöĒæ Fe2O3
”¾½āĪö”æ£Ø1£©Ć÷·Æ¾»Ė®µÄŌĄķŹĒĀČĄė×ÓĖ®½āµĆµ½ĒāŃõ»ÆĀĮ½ŗĢ壬½ŗĢåĪüø½Ė®ÖŠŌÓÖŹ£¬ĖłŅŌĄė×Ó·½³ĢŹ½ĪŖ£ŗAl3++3H2O![]() Al(OH)3£Ø½ŗĢ壩+3H+”£
Al(OH)3£Ø½ŗĢ壩+3H+”£
£Ø2£©ÅŻÄĆš»šĘ÷ÖŠ¼ÓČėµÄŹĒĢ¼ĖįĒāÄĘŗĶĮņĖįĀĮ£¬ĄūÓĆĘäĖ«Ė®½ā·“Ó¦£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗAl3++3HCO3-=Al(OH)3”ż+3CO2”ü”£
£Ø3£©Čȵēæ¼īČÜŅŗĒåĻ“ÓĶĪŪŹĒĄūÓĆĢ¼ĖįÄĘĖ®½āµĆµ½µÄ¼īÓėÓĶĪŪ·¢ÉśŌķ»Æ·“Ó¦£¬ŅŌ³żČ„ÓĶĪŪ£¬¼ÓČČŹĒĪŖĮĖ“Ł½ųĢ¼ĖįøłĄė×ÓµÄĖ®½ā£¬ŌöĒæČÜŅŗµÄ¼īŠŌ”£·“Ó¦ĪŖ£ŗCO32-+H2O![]() HCO3-+OH-”£
HCO3-+OH-ӣ
£Ø4£©¼ÓČČÕōøÉFeCl2Ė®ČÜŅŗ²¢×ĘÉÕ£¬ĀČ»ÆŃĒĢśĖ®½āµĆµ½ĒāŃõ»ÆŃĒĢśŗĶHCl,ŅņĪŖHCl»Ó·¢£¬ĖłŅŌĖ®½āĘ½ŗāŅĘ¶Æ£¬µĆµ½µÄĒāŃõ»ÆŃĒĢś±»Ńõ»ÆĪŖĒāŃõ»ÆĢś£¬·Ö½āµĆµ½Ńõ»ÆĢś”£
”¾ĢāŠĶ”æĢīæÕĢā
”¾½įŹų”æ
19
”¾ĢāÄæ”æŹµŃéĢā
£ØŅ»£©ŹµŃéŹŅÖŠÓŠŅ»Ęæŗ¬ÓŠŅ»¶ØĮæŌÓÖŹµÄÉÕ¼īѳʷ£¬Ä³Ń§ÉśÓĆÖŠŗĶµĪ¶Ø·Ø²ā¶ØÉÕ¼īµÄ“æ¶Č£¬ČōÉÕ¼īÖŠĖłŗ¬ŌÓÖŹÓėĖį²»·“Ó¦£¬Ēėøł¾ŻŹµŃé»Ų“š£ŗ
£Ø1£©½«×¼Č·³ĘČ”µÄ5gÉÕ¼īѳʷÅä³É100 mL“ż²āŅŗ£¬ŠčŅŖµÄÖ÷ŅŖŅĒĘ÷³żĮæĶ²”¢ÉÕ±”¢²£Į§°ō”¢ĶŠÅĢĢģĘ½Ķā£¬»¹±ŲŠėÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ£ŗ____________”¢_____________”£
£Ø2£©Č”10.00 mL“ż²āŅŗ£¬Ń”ŌńÓŅĶ¼ÖŠ_________£ØĢīA»ņB£©Ą“ŅĘČ””£

£Ø3£©ÓĆ0.5000mol/L±ź×¼ŃĪĖįµĪ¶Ø“ż²āÉÕ¼īČÜŅŗ£¬ŅŌ·ÓĢŖĪŖÖøŹ¾¼Į”£µĪ¶ØŹ±×óŹÖŠż×ŖµĪ¶Ø¹Ü²£Į§»īČū£¬ÓŅŹÖ²»Ķ£µŲŅ”¶Æ׶ŠĪĘ棬Į½ŃŪ×¢ŹÓ___________£¬Ö±µ½µĪ¶ØÖÕµć”£µĪ¶Ø“ļµ½ÖÕµćµÄ±źÖ¾ŹĒ£ŗ_________”£
£Ø4£©øł¾ŻĻĀĮŠŹż¾Ż£¬ÉÕ¼īµÄ“æ¶ČĪŖ£ŗ_______________________£Ø“æ¶Č=“æĪļÖŹµÄÖŹĮæ/ѳʷµÄÖŹĮæ”Į100£„£©
µĪ¶Ø“ĪŹż | “ż²āŅŗĢå»ż£ØmL£© | ±ź×¼ŃĪĖįĢå»ż£ØmL£© | |
µĪ¶ØĒ°¶ĮŹż | µĪ¶Øŗó¶ĮŹż | ||
µŚŅ»“Ī | 10.00 | 0.50 | 20.40 |
µŚ¶ž“Ī | 10.00 | 4.00 | 24.10 |
£Ø¶ž£©Ńõ»Æ»¹ŌµĪ¶ØŹµŃéÓėĖį¼īÖŠŗĶµĪ¶ØĄąĖĘ£ØÓĆŅŃÖŖÅØ¶ČµÄŃõ»Æ¼ĮČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄ»¹Ō¼ĮČÜŅŗ»ņ·“Ö®£©”£²āŃŖøʵÄŗ¬ĮæŹ±£¬½ųŠŠČēĻĀŹµŃé£ŗ
<>¢Łæɽ«2mLŃŖŅŗÓĆÕōĮóĖ®Ļ”ŹĶŗó£¬ĻņĘäÖŠ¼ÓČė×ćĮæ²ŻĖįļ§£ØNH4£©2C2O4¾§Ģ壬·“Ӧɜ³É CaC2O4³Įµķ£¬½«³ĮµķÓĆĻ”ĮņĖį“¦ĄķµĆH2C2O4ČÜŅŗ”£¢Ś½«¢ŁµĆµ½µÄH2C2O4ČÜŅŗ£¬ŌŁÓĆĖįŠŌKMnO4ČÜŅŗµĪ¶Ø£¬Ńõ»Æ²śĪļĪŖCO2£¬»¹Ō²śĪļĪŖMn2+”£
¢ŪÖÕµćŹ±ÓĆČ„20mL l.0”Įl0©4 mol/LµÄKMnO4ČÜŅŗ”£
£Ø1£©Š“³öÓĆKMnO4µĪ¶ØH2C2O4µÄĄė×Ó·½³ĢŹ½_____________________”£
£Ø2£©µĪ¶ØŹ±£¬½«KMnO4ČÜŅŗ×°ŌŚ________£ØĢī”°ĖįŹ½”±»ņ”°¼īŹ½”±£©µĪ¶Ø¹ÜÖŠ”£
£Ø3£©¼ĘĖć£ŗŃŖŅŗÖŠŗ¬øĘĄė×ÓµÄÅضČĪŖ_____mol”¤L-1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ”°ĀĢĖ®ĒąÉ½¾ĶŹĒ½šÉ½Ņųɽ”±”£ĻĀĮŠ×ö·Ø²»ĄūÓŚ±£»¤»·¾³µÄŹĒ( )
A.ĶĘ¹ćŹ¹ÓƵē¶ÆĘū³µµČµĶĢ¼½»Ķع¤¾ß
B.ĶĘ¹ćĄ¬»ų·ÖĄą£¬µē×ÓÉč±øŅŌ¾É»»ŠĀ
C.ÓĆÉśĪļ·½·ØĶŃ³żÉś»īĪŪĖ®ÖŠµÄµŖŗĶĮ×
D.¼Ó“óĒ¦ĖįŠīµē³Ų”¢ŗ¬¹ÆŠæĆĢµČµē³ŲµÄÉś²ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖA”¢BĪŖµ„ÖŹ£¬CĪŖ»ÆŗĻĪļ”£
![]()
ÄÜŹµĻÖÉĻŹö×Ŗ»Æ¹ŲĻµµÄŹĒ
¢ŁČōCČÜÓŚĖ®ŗóµĆµ½Ēæ¼īČÜŅŗ£¬ŌņAæÉÄÜŹĒNa
¢ŚČōCµÄČÜŅŗÓöNa2CO3£¬·Å³öCO2ĘųĢ壬ŌņAæÉÄÜŹĒH2
¢ŪČōCµÄČÜŅŗÖŠµĪ¼ÓKSCNČÜŅŗĻŌŗģÉ«£¬ŌņBæÉÄÜĪŖFe
¢ÜČōCµÄČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÓŠĄ¶É«³ĮµķÉś³É£¬ŌņBæÉÄÜĪŖCu
A. ¢Ł¢Ś B. ¢Ś¢Ü C. ¢Ł¢Ū D. ¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com