

| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 4 |


 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
| A、摩尔是用于计量微观粒子集体的物理量 |
| B、CO2的摩尔质量为44g |
| C、0.5mol水中约含6.02×1023个H |
| D、标准状况下1 mol任何物质体积均为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A>B>C>D |
| B、D>B>A>C |
| C、D>C>B>A |
| D、D>B>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、粗铜精炼时,与电源正极相连的是纯铜,正极反应式为:Cu2++2e-═Cu |
| D、钢铁发生电化学腐蚀的正极反应式:Fe═Fe2++2e- |
查看答案和解析>>
科目:高中化学 来源: 题型:
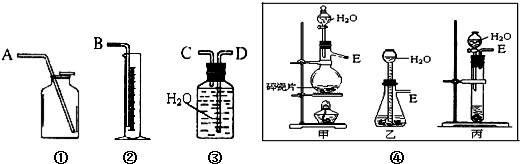
查看答案和解析>>
科目:高中化学 来源: 题型:

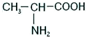 属于α-氨基酸);
属于α-氨基酸);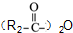 →
→ +R2COOH
+R2COOH +NaOH→R1COONa+R2NH2
+NaOH→R1COONa+R2NH2 呈弱碱性,易被氧化
呈弱碱性,易被氧化 和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 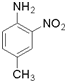 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
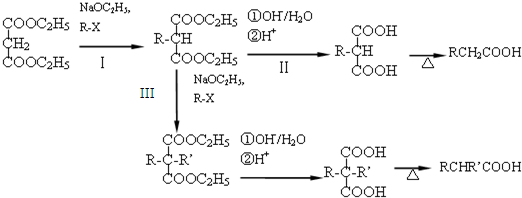
 ,所需溴代烃的结构简式为
,所需溴代烃的结构简式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com